肺高血圧症 Web Seminar
講演会に登録後、視聴サイトに遷移できない場合、ブラウザのキャッシュクリアをお試しください。キャッシュクリアの方法はこちらから確認できます。 案内状をダウンロード […]
2.1 本剤の成分に対し過敏症の既往歴のある患者
2.2 妊婦又は妊娠している可能性のある女性[9.5参照]
2.3 重度の肝機能障害(Child-Pugh分類C)のある患者[9.3.1参照]
2.4 重度の腎機能障害(クレアチニン・クリアランス15mL/min未満)のある又は透析中の患者[9.2.1、16.6.2参照]
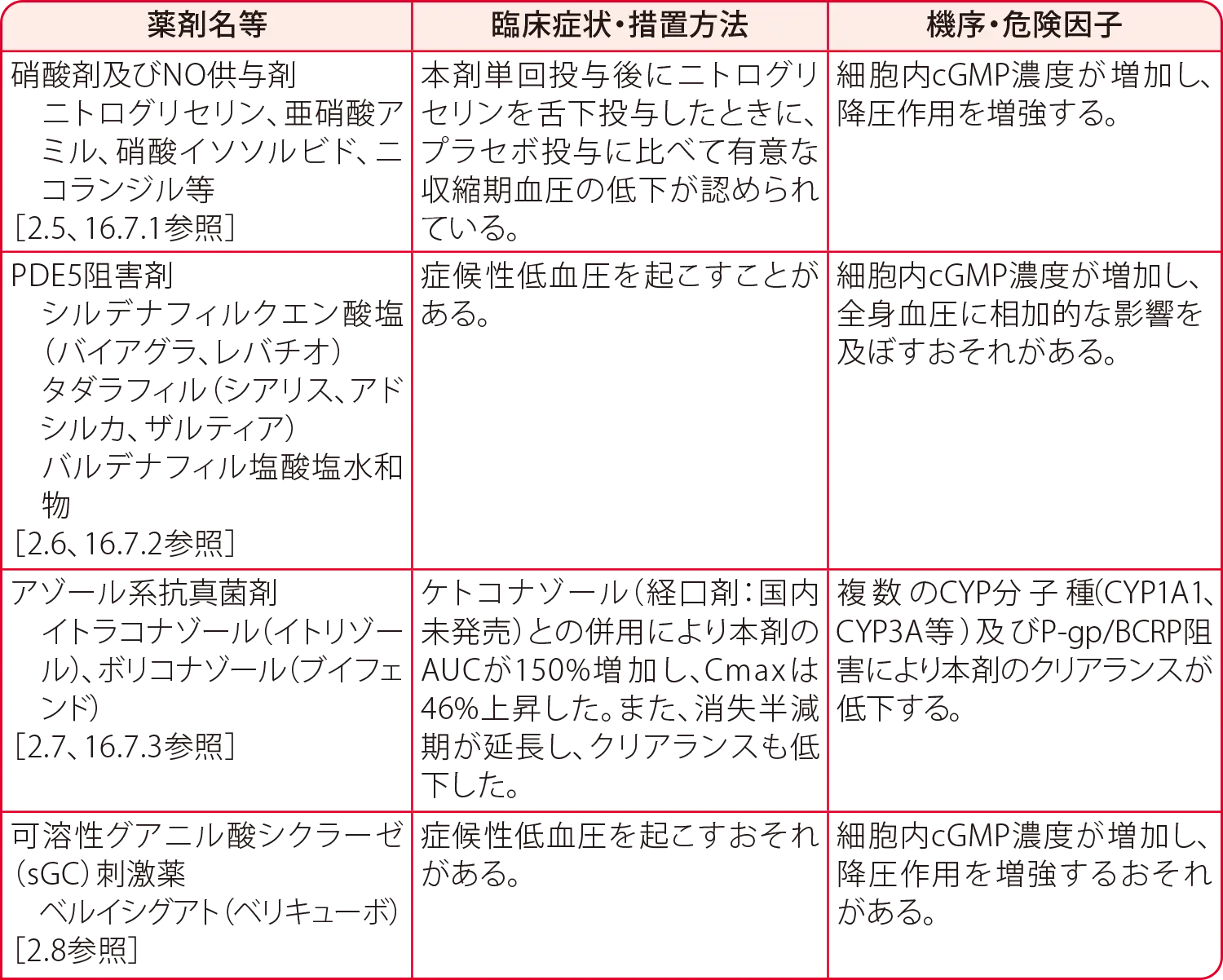
2.5 硝酸剤又は一酸化窒素(NO)供与剤(ニトログリセリン、亜硝酸アミル、硝酸イソソルビド、ニコランジル等)を投与中の患者[10.1、16.7.1参照]
2.6 ホスホジエステラーゼ(PDE)5阻害剤を投与中の患者[10.1、16.7.2参照]
2.7 アゾール系抗真菌剤(イトラコナゾール、ボリコナゾール)を投与中の患者[10.1、16.7.3参照]
2.8 可溶性グアニル酸シクラーゼ(sGC)刺激薬(ベルイシグアト)を投与中の患者[10.1参照]
〈効能共通〉
5.1 本剤の使用にあたっては、最新の慢性血栓塞栓性肺高血圧症又は肺動脈性肺高血圧症に対する治療ガイドラインを参考に投与の要否を検討すること。
〈肺動脈性肺高血圧症〉
5.2 肺動脈性肺高血圧症のWHO機能分類クラスⅣにおける有効性及び安全性は確立していない。
用量調節期
通常、成人にはリオシグアトとして1回1.0mg 1日3回経口投与から開始する。2週間継続して収縮期血圧が95mmHg以上で低血圧症状を示さない場合には、2週間間隔で1回用量を0.5mgずつ増量するが、最高用量は1回2.5mg 1日3回までとする。収縮期血圧が95mmHg未満でも低血圧症状を示さない場合は、現行の用量を維持するが、低血圧症状を示す場合には、1回用量を0.5mgずつ減量する。
用量維持期
用量調節期に決定した用量を維持する。用量維持期においても、最高用量は1回2.5mg 1日3回までとし、低血圧症状を示すなど、忍容性がない場合には、1回用量を0.5mgずつ減量する。
7.1 患者の状態に応じて1回1.0mg 1日3回より低用量からの開始も考慮すること。[9.1.2、9.2.2、9.3.2、9.8、10.2参照]
7.2 投与間隔は約6~8時間間隔とすることが望ましい。ただし、1回の服用を忘れた場合には、次回の服用時刻に1回用量を服用させる。
7.3 3日間以上投与が中断した場合、再開時には、開始時の用量を考慮し、「6. 用法及び用量」に従い用量調節を行う。
8.1 本剤の投与により肺水腫の徴候がみられた場合には、肺静脈閉塞性疾患との関連性を疑い、投与を中止すること。[9.1.3参照]
8.2 本剤は血管を拡張して血圧を低下させる作用を有している。本剤の投与に際しては、血管拡張作用により患者が有害な影響を受ける状態(降圧剤投与中、安静時低血圧、血液量減少、重度の左室流出路閉塞、自律神経機能障害等)にあるかどうかを十分検討すること。
8.3 臨床試験において、めまい等が認められているので、高所作業、自動車の運転等危険を伴う機械を操作する際には注意させること。
8.4 特発性間質性肺炎に伴う症候性肺高血圧症を対象とした国際共同試験において、本剤投与群ではプラセボ投与群と比較して重篤な有害事象及び死亡が多く認められた。間質性肺病変を伴う肺動脈性肺高血圧症の患者に本剤を投与する場合は、間質性肺疾患の治療に精通した専門医に相談するなど、本剤投与によるリスクとベネフィットを考慮した上で、投与の可否を慎重に検討すること。[15.1参照]
9.1 合併症・既往歴等のある患者
9.1.1 抗凝固療法中の患者
気道出血が起こる可能性が高くなるため、喀血が起こりやすく、重篤で致死的な喀血の危険性が高まる可能性がある。患者ごとに本剤投与のリスク・ベネフィットを定期的に評価すること。[11.1参照]
9.1.2 投与前の収縮期血圧が95mmHg未満の患者
過度の血圧低下が起こるおそれがある。本剤の投与に際しては、患者における治療上のリスク・ベネフィットを考慮して慎重に判断すること。国際共同第Ⅲ相試験では除外されている。[7.1参照]
9.1.3 肺静脈閉塞性疾患の患者
本剤を投与しないことが望ましい。心血管系の状態を著しく悪化させるおそれがある。[8.1参照]
9.1.4 喫煙者
禁煙させることが望ましい。非喫煙者に比べて本剤の血漿中濃度が低下する。[16.6.1参照]
9.2 腎機能障害患者
9.2.1 重度の腎機能障害患者又は透析中の患者
クレアチニン・クリアランス15mL/min未満の患者又は透析中の患者には投与しないこと。血中濃度が著しく上昇するおそれがある。国際共同第Ⅲ相試験では除外されている。[2.4、16.6.2参照]
9.2.2 軽度又は中等度の腎機能障害患者
1回0.5mg 1日3回からの開始も考慮すること。クレアチニン・クリアランス15~80mL/min未満の患者では血中濃度が上昇する。[7.1、16.6.2参照]
9.3 肝機能障害患者
9.3.1 重度の肝機能障害患者
Child-Pugh分類Cの患者には投与しないこと。血中濃度が著しく上昇するおそれがある。国際共同第Ⅲ相試験では除外されている。[2.3参照]
9.3.2 軽度又は中等度の肝機能障害患者
Child-Pugh分類A又はBの患者では血中濃度が上昇する。[7.1、16.6.3参照]
9.4 生殖能を有する者
妊娠する可能性のある女性に以下について説明及び指導し、必要に応じて妊娠検査を行い、妊娠していないことを確認すること。[9.5参照]
・妊娠中に本剤を服用した場合に胎児に影響を及ぼす危険性があること。
・本剤の服用開始後は確実な避妊法を用いること。
・妊娠した場合若しくはその疑いがある場合には、直ちに医師に連絡すること。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には投与しないこと。動物実験において、ラットで心室中隔欠損、骨化遅延(胸骨分節)及び全胚吸収がヒトの8.1倍の全身曝露量で発現することが報告されている1)。また、ウサギで流産及び全胚吸収がそれぞれヒトの3.8倍及び12.6倍の全身曝露量で発現することが報告されている2)。[2.2、9.4参照]
9.6 授乳婦
授乳しないことが望ましい。動物実験(ラット、経口投与)で乳汁中に投与量の2.2%が移行することが報告されている3)。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
血中濃度の上昇が認められている。[7.1、16.6.4参照]
本剤は、主にCYP1A1、CYP2C8、CYP2J2及びCYP3Aにより代謝される。本剤はP-糖タンパク/乳癌耐性タンパク(P-gp/BCRP)の基質であるため、これらの阻害薬若しくは誘導薬により血漿中濃度が影響を受ける可能性がある。また、本剤及び主代謝物M-1はCYP1A1阻害作用がある(in vitro)。
10.1 併用禁忌(併用しないこと)
10.2 併用注意(併用に注意すること)

次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1 重大な副作用
11.1.1 喀血(0.2%)、肺出血(頻度不明)
[9.1.1参照]
11.2 その他の副作用

1)社内資料: ラットにおける胚・胎児発生に関する毒性試験(2014年1月17日承認、CTD2.6.6.6.2)
2)社内資料: ウサギにおける胚・胎児発生に関する毒性試験(2014年1月17日承認、CTD2.6.6.6.3)
3)社内資料: ラットにおける乳汁中分泌に関する試験(2014年1月17日承認、CTD2.6.4.6.4)
4)DeJesus E, et al.: Pulm Circ. 2019; 9: 1-10
2024年1月改訂(第3版)
「効能又は効果」、「用法及び用量」、「禁忌を含む使用上の注意」、「効能又は効果に関連する注意」、「用法及び用量に関連する注意」、「副作用」等詳細については、電子添文をご参照ください。

講演会に登録後、視聴サイトに遷移できない場合、ブラウザのキャッシュクリアをお試しください。キャッシュクリアの方法はこちらから確認できます。 案内状をダウンロード […]

講演会に登録後、視聴サイトに遷移できない場合、ブラウザのキャッシュクリアをお試しください。キャッシュクリアの方法はこちらから確認できます。 案内状をダウンロード […]

講演会に登録後、視聴サイトに遷移できない場合、ブラウザのキャッシュクリアをお試しください。キャッシュクリアの方法はこちらから確認できます。 案内状をダウンロード […]
WEB講演会にアクセスし「このページは閲覧を制限しています」と表示された方は こちら>>
このサイトでは、医療用医薬品を適正にご使用いただくため、医師、歯科医師及び薬剤師などの医療関係者の方を対象に、主としてMSD株式会社の医療用医薬品に関する情報を提供しています。
下記の「はい」をクリックした場合、「MSD Connect ご利用規約」及び「ウェブサイトのご利用条件」を理解したうえで、内容に同意したものとみなします。
2024年11月にご利用規約を改訂致しました。上記リンクよりご確認ください。
あなたは医療関係者ですか?