薬物動態:血漿中濃度
薬物動態:血漿中濃度
錠剤
1. 単回投与1)
日本人健康成人女性に、レテルモビル240mg及び480mgを空腹時単回経口投与した際、レテルモビルは投与後2.25~3.00時間で最高血漿中濃度に到達し、その後、二相性の消失を示しました。レテルモビルのAUC0-∞は、用量比を上回る上昇を示しました。
■日本人健康成人女性にレテルモビルを空腹時単回経口投与した際の薬物動態パラメータ
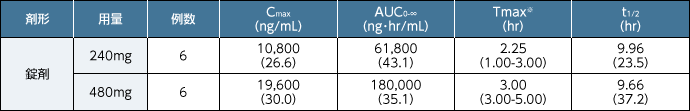
幾何平均(幾何平均に基づく変動係数[%])
※:中央値(範囲)
2. 反復投与2)
日本人健康成人女性に、レテルモビル480mgを反復経口投与した際、AUC0-24hr及びCmaxの幾何平均比に基づく累積係数は、それぞれ0.97及び0.94でした。
■日本人健康成人女性にレテルモビル480mgを1日1回7日間反復経口投与した際の血漿中レテルモビル濃度推移及び薬物動態パラメータ
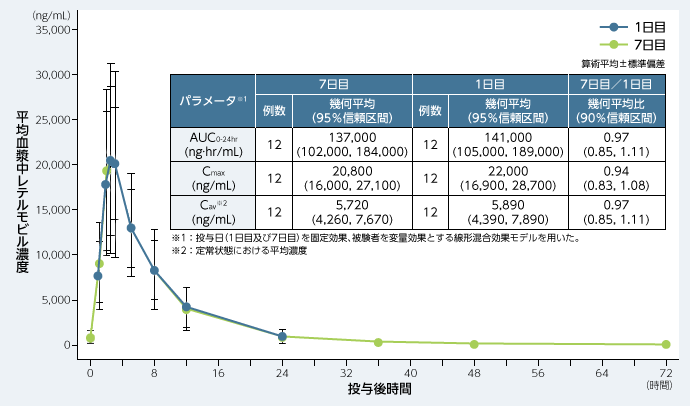
3. 成人同種造血幹細胞移植患者(日本人及び外国人データ)3)
成人同種造血幹細胞移植患者350例(うち、日本人成人同種造血幹細胞移植患者23例)から得られた血漿中レテルモビル濃度データを用いて、母集団薬物動態解析を実施しました。日本人成人同種造血幹細胞移植患者にレテルモビルを480mg、及びシクロスポリンを併用投与する場合はレテルモビルを240mgで1日1回経口投与した際の、レテルモビルの定常状態におけるAUC0-24hrは、それぞれ42,390、66,450ng·hr/mLでした。第Ⅲ相国際共同試験(001試験)で得られた曝露量の範囲では、一貫した有効性が示されており、各投与方法における曝露量に、臨床的な違いは認められませんでした。
■日本人成人同種造血幹細胞移植患者にレテルモビル480mg、及びシクロスポリンを併用投与する場合はレテルモビル240mgで1日1回経口投与した際の定常状態におけるAUC0-24hr
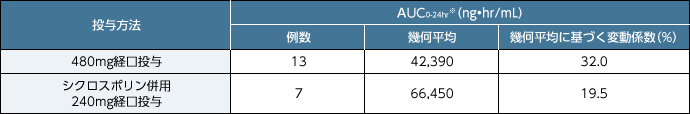
※:日本人成人同種造血幹細胞移植患者の血漿中レテルモビル濃度データを用いた母集団薬物動態解析から得られたAUC0-24hrのベイズ推定値
4. 成人腎移植患者(日本人及び外国人データ)4、5)
成人腎移植患者を対象とした海外第Ⅲ相試験(002試験)における薬物動態学的特徴について、母集団薬物動態解析を用いて評価したところ、非日本人成人腎移植患者に対してレテルモビル480mgを経口投与した際の定常状態におけるAUC0-24の推定値は、中央値で62,200ng·hr/mL、レテルモビル240mgをシクロスポリンと併用して経口投与した際のレテルモビルのAUC0-24の推定値は、中央値で57,700ng·hr/mLでした。
日本人成人腎移植患者を対象としてレテルモビル480mgを経口投与した国内第Ⅲ相試験において、ノンコンパートメント解析による定常状態のAUC0-24の幾何平均値は156,000ng·hr/mL、Cmaxは17,900ng/mLであり、日本人成人腎移植患者の曝露量は非日本人成人腎移植患者と比較して高値を示しました。日本人成人腎移植患者の体重[算術平均±標準偏差(例数):63.8±12.4kg(n=22)]は、非日本人成人腎移植患者の体重[82.7±19.1kg(n=292)]よりも低く、曝露量の差の主要な要因として体重差の影響が考えられました。
■非日本人成人腎移植患者を対象とした海外第Ⅲ相試験(002試験)におけるレテルモビルのAUCのベイズ推定値の要約
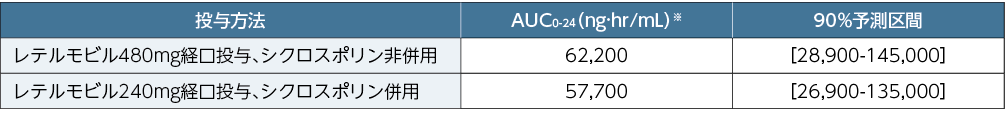
※:定常状態における中央値[90%予測区間]で、母集団PK解析によりベイズ推定したAUC。
各値は有効数字3桁に四捨五入した。
■成人腎移植患者に本剤480mgを反復経口投与した国内外の第Ⅲ相試験(042試験、002試験)の定常状態における曝露量

※1:幾何平均値(幾何平均値に基づく変動係数%)、各値は有効数字3桁に四捨五入した。
※2:定常状態における中央値[90%予測区間]で、母集団PK解析によりベイズ推定したAUC。002試験で得られたAUCの範囲は、14,300~259,000ng·hr/mLであった。
※3:吸収相のデータが十分にないため、算出しなかった。
5. 食事の影響(外国人データ)6)
外国人健康成人女性に、高脂肪・高カロリー食摂取後にレテルモビル480mgを単回経口投与した際、空腹時投与と比較して、レテルモビルのCmaxは約30%上昇したものの、AUCは変わりませんでした。
■外国人健康成人女性にレテルモビル480mgを食後と空腹時に単回経口投与した際の薬物動態パラメータ
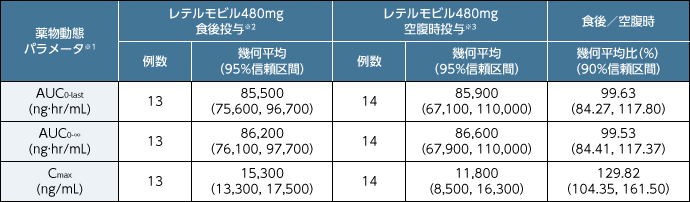
※1:自然対数変換後、線形混合効果モデルにより計算した最小二乗平均及び信頼区間の逆変換値
※2:高脂肪・高カロリー食摂取開始後30分にレテルモビル480mgを単回経口投与した。
※3:10時間以上の絶食後にレテルモビル480mgを単回経口投与した。
錠剤 顆粒剤
1. 錠剤及び顆粒剤の相対的バイオアベイラビリティ(外国人データ)7)
非日本人健康成人女性に、レテルモビル錠240mg又はレテルモビル顆粒240mgのいずれかを空腹時に単回経口投与したところ、AUC0-inf及びCmaxは錠剤と顆粒剤で類似しており、生物学的同等性の基準を満たしていました。
また、レテルモビル顆粒240mgを空腹時に単独又は軟らかい食品(バニラプリンあるいはアップルソース)と混合して単回投与した結果は以下の通りでした。
■非日本人健康成人女性にレテルモビル240mgを顆粒剤又は錠剤として投与した際のAUC0-inf及びCmax
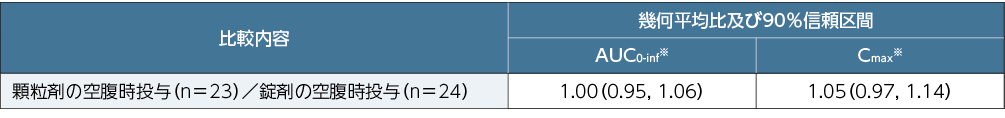
※:自然対数変換後に線形混合効果モデルにより計算した最小二乗平均及び信頼区間の逆変換値
■非日本人健康成人女性にレテルモビル240mgの顆粒剤を軟らかい食品とともに投与又は単独で投与した際のAUC0-inf及びCmax
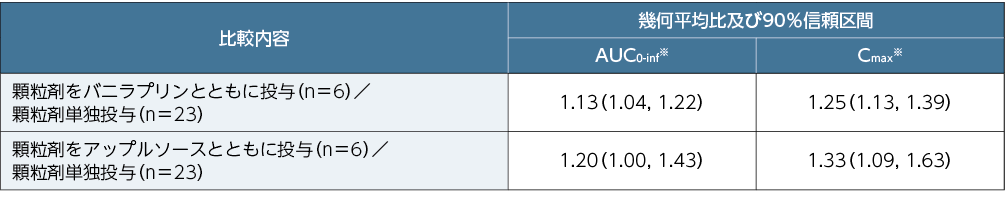
※:自然対数変換後に線形混合効果モデルにより計算した最小二乗平均及び信頼区間の逆変換値
2. 小児同種造血幹細胞移植患者(日本人及び外国人データ)8)
小児同種造血幹細胞移植患者60例(うち、日本人小児同種造血幹細胞移植患者4例)から得られた血漿中レテルモビル濃度データを用いて、母集団薬物動態解析を実施しました。小児同種造血幹細胞移植患者にレテルモビル1日1回経口投与した際の、レテルモビルの定常状態におけるAUC0-24hrは、体重別にレテルモビルの投与量を設定することで、成人同種造血幹細胞移植患者で得られた曝露量の範囲内になることが予測されました。
■小児同種造血幹細胞移植患者にレテルモビル1日1回経口投与した際の定常状態における予測AUC0-24hr
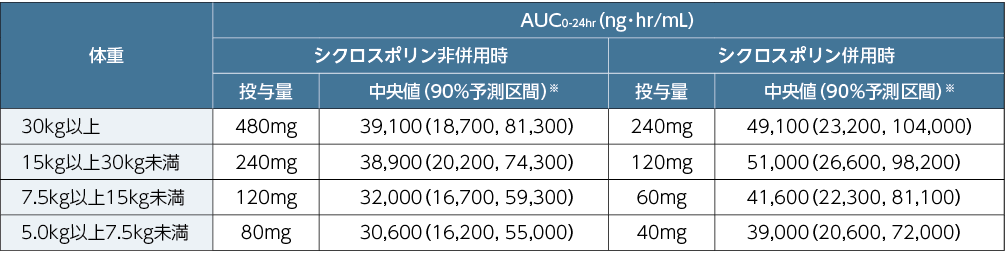
※:中央値及び90%予測区間は、小児同種造血幹細胞移植患者の母集団薬物動態モデルを用いた個体間変動を考慮したシミュレーションに基づき算出した。
点滴静注
1. 単回投与1)
日本人健康成人女性にレテルモビル240mg及び480mgを60分かけて単回静脈内投与した際の、レテルモビルの薬物動態パラメータは以下の通りでした。レテルモビルは、二相性の消失を示しました。また、レテルモビルのAUC0-∞は、用量比を上回る上昇を示しました。
■日本人健康成人女性にレテルモビルを単回静脈内投与した際の薬物動態パラメータ
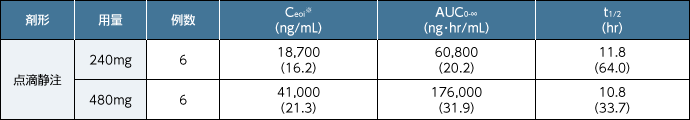
幾何平均(幾何平均に基づく変動係数[%])
※:静脈内投与終了時の血漿中濃度
2. 反復投与(外国人データ)9)
外国人健康成人女性にレテルモビル480mgを60分かけて静脈内に反復投与したときの、レテルモビルのAUC0-24hr及びAUC0-12hrの幾何平均比に基づく累積係数は、それぞれ1.22及び1.17でした。Ceoiに累積はみられず、幾何平均比に基づく累積係数は1.06でした。
■外国人健康成人女性にレテルモビル480mgを60分かけて1日1回7日間反復静脈内投与した際の累積係数の推定値
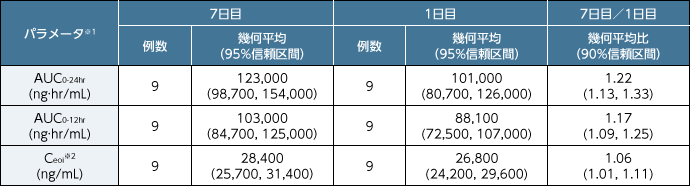
※1:自然対数変換後の値に対して投与日を固定効果、被験者を変量効果とする線形混合効果モデルで解析した。最小二乗平均及び最小二乗平均の差を逆変換し、幾何平均、幾何平均比とそれらの信頼区間を示した。
※2:静脈内投与終了時の血漿中濃度
3. 成人同種造血幹細胞移植患者(日本人及び外国人データ)3)
成人同種造血幹細胞移植患者350例(うち、日本人成人同種造血幹細胞移植患者23例)から得られた血漿中レテルモビル濃度データを用いて、母集団薬物動態解析を実施しました。日本人成人同種造血幹細胞移植患者にレテルモビルを480mg、シクロスポリンを併用投与する場合はレテルモビルを240mgで1日1回静脈内投与した際の、レテルモビルの定常状態におけるAUC0-24hrは、それぞれ101,200、70,810ng·hr/mLでした。第Ⅲ相国際共同試験(001試験)で得られた曝露量の範囲では、一貫した有効性が示されており、各投与方法における曝露量に、臨床的な違いは認められませんでした。
■日本人成人同種造血幹細胞移植患者にレテルモビル480mg、及びシクロスポリンを併用投与する場合はレテルモビル240mgで1日1回静脈内投与した際の定常状態におけるAUC0-24hr
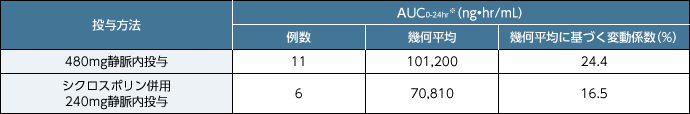
※:日本人成人同種造血幹細胞移植患者の血漿中レテルモビル濃度データを用いた母集団薬物動態解析から得られたAUC0-24hrのベイズ推定値
4. 小児同種造血幹細胞移植患者(日本人及び外国人データ)8)
小児同種造血幹細胞移植患者60例(うち、日本人小児同種造血幹細胞移植患者4例)から得られた血漿中レテルモビル濃度データを用いて、母集団薬物動態解析を実施しました。小児同種造血幹細胞移植患者にレテルモビル1日1回静脈内投与した際の、レテルモビルの定常状態におけるAUC0-24hrは、体重別にレテルモビルの投与量を設定することで、成人同種造血幹細胞移植患者で得られた曝露量の範囲内になることが予測されました。
■小児同種造血幹細胞移植患者にレテルモビル1日1回静脈内投与した際の定常状態における予測AUC0-24hr
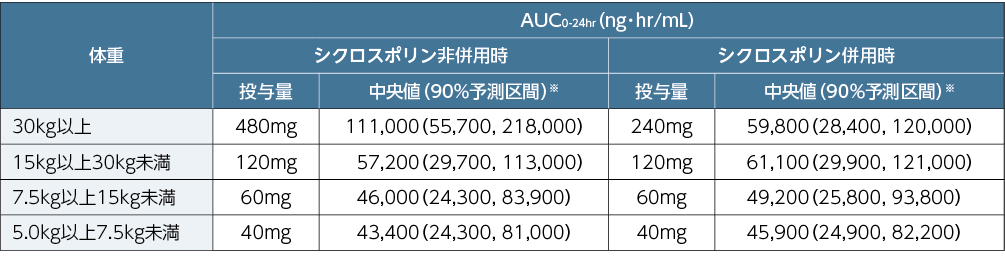
※:中央値及び90%予測区間は、小児同種造血幹細胞移植患者の母集団薬物動態モデルを用いた個体間変動を考慮したシミュレーションに基づき算出した。
4. 効能又は効果
下記におけるサイトメガロウイルス感染症の発症抑制
〇同種造血幹細胞移植
〇臓器移植
6. 用法及び用量
・錠240mg 顆粒分包20mg・120mg
通常、成人にはレテルモビルとして480mg(240mg錠2錠又は120mg顆粒4包)を1日1回経口投与する。シクロスポリンと併用投与する場合にはレテルモビルとして240mg(240mg錠1錠又は120mg顆粒2包)を1日1回経口投与する。
通常、小児にはレテルモビルとして以下の用量を1日1回経口投与する。
・点滴静注240mg
通常、成人にはレテルモビルとして480mgを1日1回、約60分かけて点滴静注する。シクロスポリンと併用投与する場合にはレテルモビルとして240mgを1日1回、約60分かけて点滴静注する。
通常、小児にはレテルモビルとして以下の用量を1日1回、約60分かけて点滴静注する。
1)承認時評価資料(健康成人における単回経口及び静脈内投与試験:027試験)
2)承認時評価資料(健康成人における反復経口投与及びシクロスポリンとの薬物相互作用:032試験)
3)社内資料(第Ⅲ相臨床試験データを用いた母集団薬物動態(PPK)解析、成人同種造血幹細胞移植患者)
4)適応追加(臓器移植)承認時評価資料(第Ⅲ相国内試験:042試験)
5)社内資料(第Ⅲ相臨床試験データを用いた母集団薬物動態(PPK)解析、成人腎移植患者)
6)承認時評価資料(外国人健康成人における食事の影響試験:029試験)
7)承認時評価資料(健康成人を対象に成人用製剤に対する顆粒剤2種類の相対的バイオアベイラビリティ試験:031試験)
8)社内資料(後期第Ⅱ相臨床試験データを用いた母集団薬物動態(PPK)解析、小児同種造血幹細胞移植患者)
9)社内資料(外国人健康成人を対象とした反復経口及び静脈内投与試験:026試験)