臨床成績
「警告・禁忌を含む注意事項等情報」等は電子添文をご参照ください。
臨床成績
1.ベクロニウム臭化物を対照とした比較試験(国内第Ⅲ相試験)1,2)
1)社内資料:ベクロニウム臭化物を対照としたOrg9426の検証的試験(第Ⅲ相)(71101試験、承認時評価資料)
2)新宮 興, 他. 麻酔 2006; 55(9): 1140-1148. [利益相反:本試験は日本オルガノン(現MSD)の支援により行われた。]
[試験概要]
目的:セボフルラン麻酔下で一般的な手術を受ける患者において、エスラックス®0.6又は0.9mg/kgあるいはベクロニウム臭化物0.1mg/kgを挿管用量として投与したときの有効性及び安全性を比較検討する。
試験デザイン:第Ⅲ相、多施設、無作為化、非盲検試験
対象:手術患者88例(ASA分類Class 1~3、20~65歳未満、手術予定時間1.5~3時間)
エスラックス®0.6mg/kg群:30例、エスラックス®0.9mg/kg群:28例、ベクロニウム臭化物0.1mg/kg群:30例
投与方法:
麻酔導入:100%酸素吸入下でプロポフォールにより麻酔導入。必要に応じてさらにプロポフォール、フェンタニル、ドロペリドールを適宜投与。
麻酔維持:亜酸化窒素と酸素(原則として2: 1)にセボフルランを0. 5~2%の濃度で投与開始し、麻酔深度を調節。
1回目の追加ボーラス投与時の作用持続時間の測定が完了するまで、呼気中のセボフルラン濃度を2%に調節。
エスラックス®:挿管用量として0.6mg/kg又は0.9mg/kgを静脈内投与。筋弛緩の維持のために0.1、0.15又は0.2mg/kgを追加ボーラス投与。
ベクロニウム臭化物:挿管用量として0.1mg/kgを静脈内投与。筋弛緩の維持のために0.025mg/kgを追加ボーラス投与した。
評価項目:
主要評価項目:作用発現時間(筋弛緩薬投与完了からT1の最大遮断が得られるまでの時間)
副次評価項目:作用持続時間(筋弛緩薬投与完了からT1がコントロールの25%に回復するまでの時間)
90%遮断時間(筋弛緩薬投与完了からT1が90%遮断されるまでの時間)等
安全性
解析計画:すべての有効性解析はIntent-To-Treat(ITT)グループ及び治験実施計画書に適合した解析対象(PP)グループについて行った。主要評価項目の作用発現時間については、t-検定により逐次的に行った。
副次評価項目の作用持続時間については、主要評価項目と同様に解析を行った。
また、維持用量投与後における作用持続時間の用量反応性について直線回帰分析を行った。
有効性
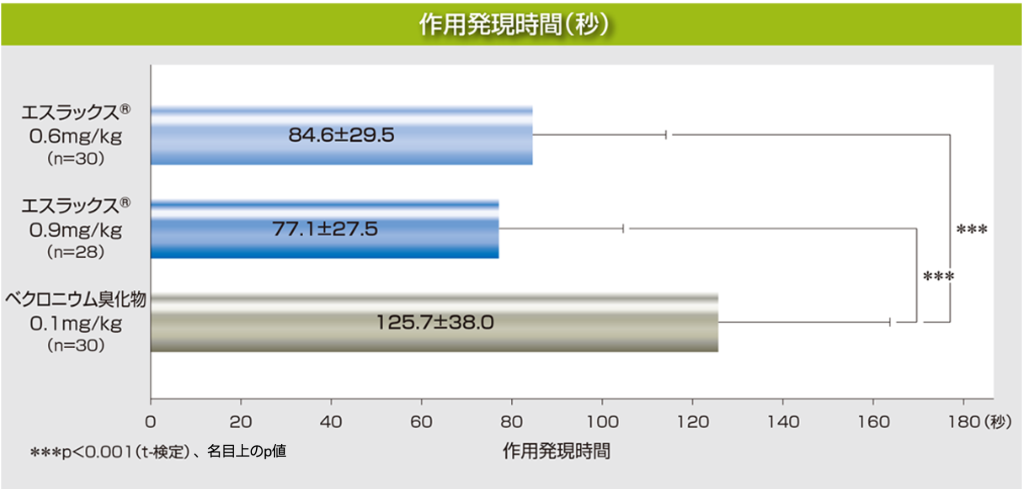
【1】作用発現時間[主要評価項目]
挿管用量としてエスラックス®0.6mg/kg又は0.9mg/kg、ベクロニウム臭化物0.1mg/kgを投与した時の作用発現時間(筋弛緩薬投与完了からT1*の最大遮断が得られるまでの時間)の平均値は、それぞれ84.6秒、77.1秒、125.7秒で、エスラックス®0.6mg/kg群、0.9mg/kg群ともにベクロニウム臭化物群に比べて有意に速いことが認められました(いずれもp<0.001、t-検定)。
*T1:0.5秒間隔の連続4回の電気刺激の第一反応(Twitch)
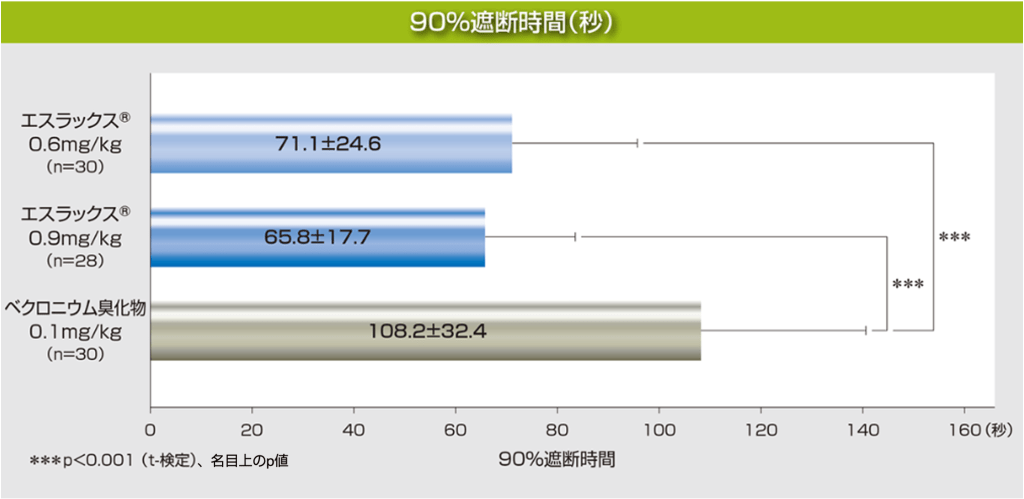
【2】90%遮断時間[副次評価項目]
挿管用量としてエスラックス®0.6mg/kg又は0.9mg/kg、ベクロニウム臭化物0.1mg/kgを投与した時の90%遮断時間(筋弛緩剤投与完了からT1が90%遮断されるまでの時間)の平均値は、それぞれ71.1秒、65.8秒、108.2秒で、エスラックス®0.6mg/kg群、0.9mg/kg群ともにベクロニウム臭化物群に比べて有意に速いことが認められました(いずれもp<0.001 、t-検定)。
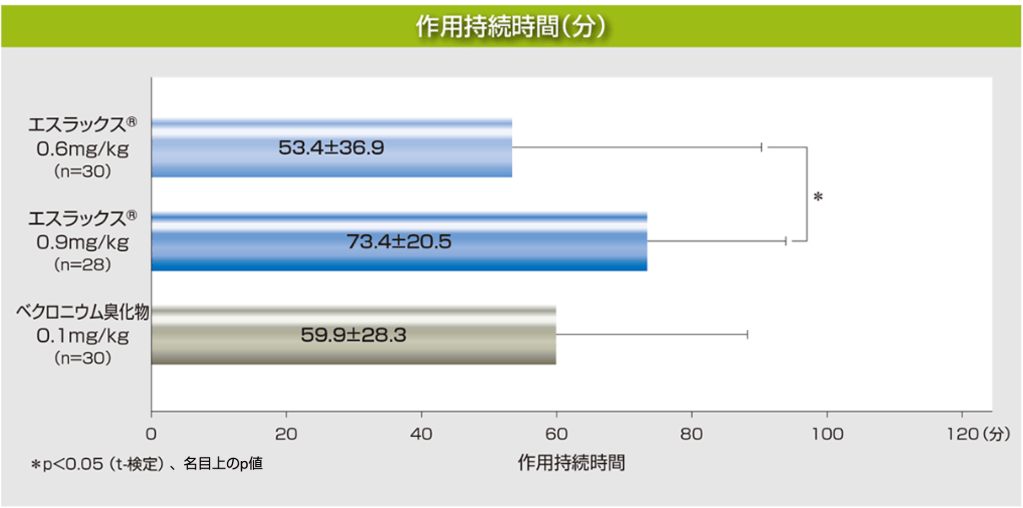
【3】作用持続時間[副次評価項目]
挿管用量としてエスラックス®0.6mg/kg又は0.9mg/kg、ベクロニウム臭化物0.1mg/kgを投与した時の作用持続時間(筋弛緩薬投与完了からT1がコントロールの25%に回復するまでの時間)の平均値は、それぞれ53.4分、73.4分、59.9分で、エスラックス®0.6mg/kg群、0.9mg/kg群ともベクロニウム臭化物群との間に有意差は認められませんでした(t-検定)。
なお、本試験において、エスラックス®0.6mg/kg群及び0.9mg/kg群の1回目維持用量と作用持続時間との用量反応性を検討した結果、直線回帰モデルにおいていずれの用量でも有意な相関が認められました(p=0.0001及びp=0.0500)。
安全性
エスラックス®又はベクロニウム臭化物との関連性が認められた有害事象は、エスラックス®0.6mg/kg群6.7%(2/30例)、エスラックス®0.9mg/kg群7. 1%(2/28例)、ベクロニウム臭化物0.1mg/kg群23.3%(7/30例)であった。主な事象は、エスラックス®0.6mg/kg群で浮動性めまい、徐脈、低血圧、上腹部痛、接触性皮膚炎(各1例, 各3.3%)、エスラックス®0.9mg/kg群で心室性期外収縮、発疹(各1例, 各3.6%)、ベクロニウム臭化物0.1mg/kg群で悪心(4例, 13.3%)、房室解離(1例, 3.3%)等であった。各群において死亡及び重篤な有害事象、中止に至った有害事象は認められなかった。
エスラックス®の用法及び用量
6.用法及び用量
通常、成人には挿管用量としてロクロニウム臭化物0.6mg/kgを静脈内投与し、術中必要に応じて0.1~0.2mg/kgを追加投与する。持続注入により投与する場合は、7μg/kg/分の投与速度で持続注入を開始する。なお、年齢、症状に応じて適宜増減するが、挿管用量の上限は0.9mg/kgまでとする。
7.用法及び用量に関連する注意(抜粋)
7.1 作用持続時間は用量に依存して長くなるため、本剤0.9mg/kgを挿管用量として投与する際は注意すること。
10.相互作用(抜粋)
10.2 併用注意(併用に注意すること)
吸入麻酔剤セボフルラン:本剤の筋弛緩作用が増強されることがあるので、併用する場合には減量するなど注意すること。