KEYNOTE-189試験(最終解析)
国際共同第Ⅲ相試験:KEYNOTE-189試験(最終解析)
主要評価項目 最終解析での全生存期間:OS
全生存期間(OS)のKaplan-Meier曲線(ITT集団)
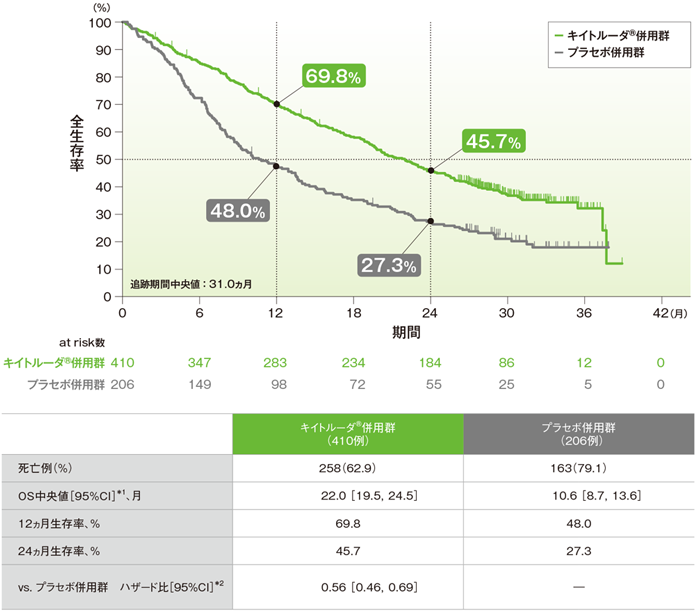
*1 打ち切りデータはproduct-limit(Kaplan-Meier)法に基づく
*2 投与群を共変量とし、PD-L1発現(≥1%、<1%)、プラチナ製剤(シスプラチン、カルボプラチン)、喫煙歴(喫煙歴なし、現喫煙者/喫煙歴あり)を層別因子とした層別Cox比例ハザードモデルに基づく
(追跡期間中央値:31.0ヵ月)(データカットオフ日:2019年5月20日)
Rodríguez-Abreu D et al. Ann Oncol 2021; 32: 881-895
本試験はMSD社の資金提供により行われた。
OS中央値は、キイトルーダ®併用群で22.0ヵ月(95%CI:19.5, 24.5)、プラセボ併用群で10.6ヵ月(95%CI:8.7, 13.6)でした。
探索的評価項目(サブグループ解析) 最終解析でのPD-L1発現別の全生存期間:OS
PD-L1発現陰性患者(TPS<1%)における全生存期間(OS)のKaplan-Meier曲線(ITT集団)
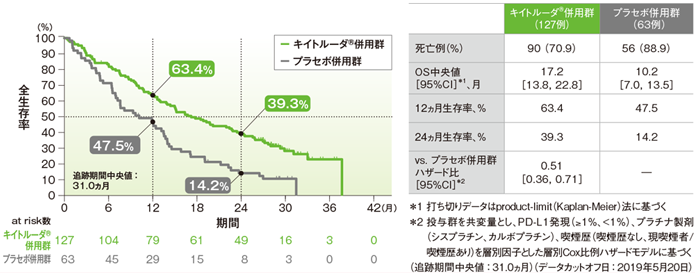
PD-L1低発現患者(TPS 1-49%)における全生存期間(OS)のKaplan-Meier曲線(ITT集団)
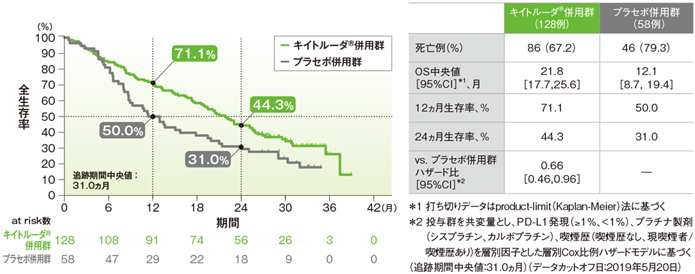
PD-L1高発現患者(TPS≥50%)における全生存期間(OS)のKaplan-Meier曲線(ITT集団)
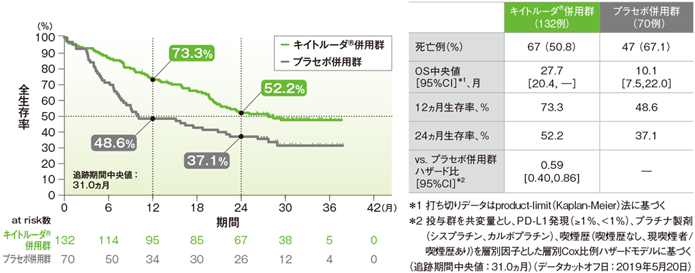
Rodríguez-Abreu D et al. Ann Oncol 2021; 32: 881-895
本試験はMSD社の資金提供により行われた。
サブグループ解析 最終解析での部分集団因子別の全生存期間:OS
全生存期間(OS)のハザード比のフォレストプロット(ITT集団)
*投与群を共変量とし、PD-L1発現(≥1%、<1%)、プラチナ製剤(シスプラチン、カルボプラチン)、喫煙歴(喫煙歴なし、現喫煙者/喫煙歴あり)を層別因子とした層別Cox比例ハザードモデルに基づく
(追跡期間中央値:31.0ヵ月)(データカットオフ日:2019年5月20日)
Rodríguez-Abreu D et al. Ann Oncol 2021; 32: 881-895
本試験はMSD社の資金提供により行われた。
主要評価項目 最終解析での無増悪生存期間:PFS
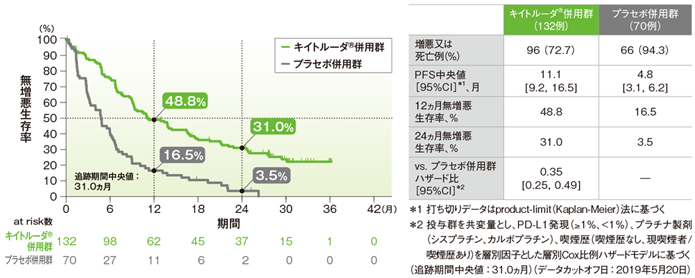
無増悪生存期間(PFS)のKaplan-Meier曲線(ITT集団)
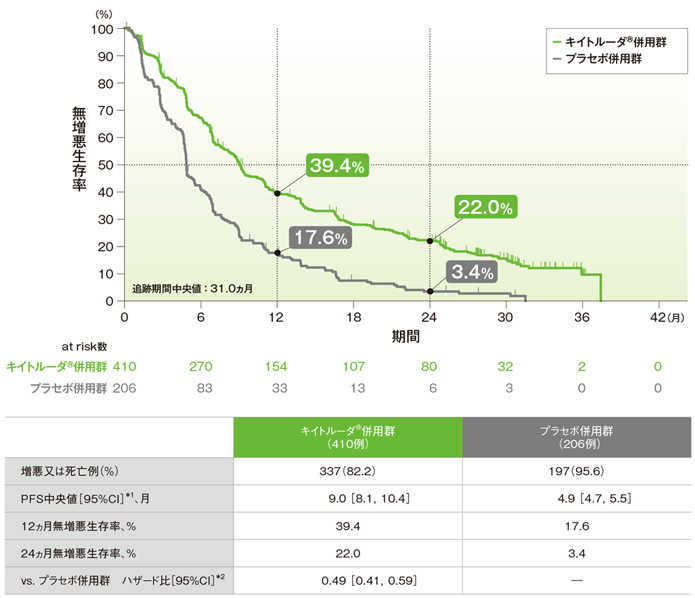
*1 打ち切りデータはproduct-limit(Kaplan-Meier)法に基づく
*2 投与群を共変量とし、PD-L1発現(≥1%、<1%)、プラチナ製剤(シスプラチン、カルボプラチン)、喫煙歴(喫煙歴なし、現喫煙者/喫煙歴あり)を層別因子とした層別Cox比例ハザードモデルに基づく
(追跡期間中央値:31.0ヵ月)(データカットオフ日:2019年5月20日)
Rodríguez-Abreu D et al. Ann Oncol 2021; 32: 881-895
本試験はMSD社の資金提供により行われた。
PFS中央値は、キイトルーダ®併用群で9.0ヵ月(95%CI:8.1, 10.4)、プラセボ併用群で4.9ヵ月(95%CI:4.7, 5.5)でした。
探索的評価項目(サブグループ解析) 最終解析でのPD-L1発現別の無増悪生存期間:PFS
PD-L1発現陰性患者(TPS<1%)における無増悪生存期間(PFS)のKaplan-Meier曲線(ITT集団)
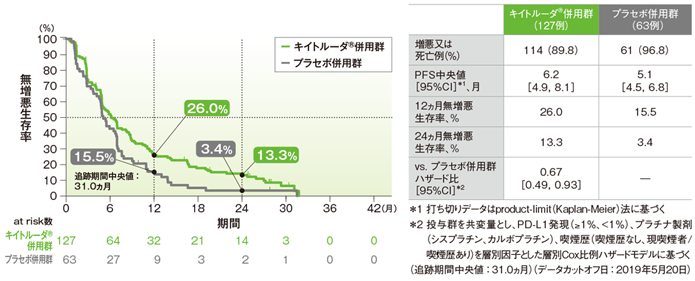
PD-L1低発現患者(TPS 1-49%)における無増悪生存期間(PFS)のKaplan-Meier曲線(ITT集団)
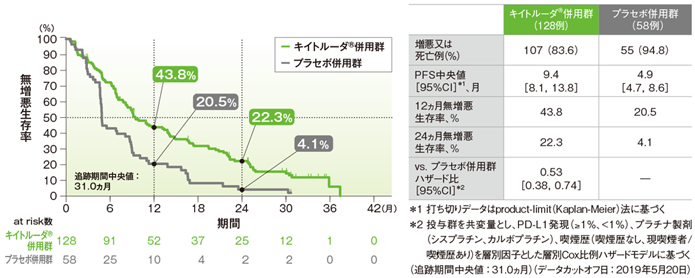
PD-L1高発現患者(TPS≥50%)における無増悪生存期間(PFS)のKaplan-Meier曲線(ITT集団)
Rodríguez-Abreu D et al. Ann Oncol 2021; 32: 881-895
本試験はMSD社の資金提供により行われた。
サブグループ解析 最終解析での部分集団因子別の無増悪生存期間:PFS
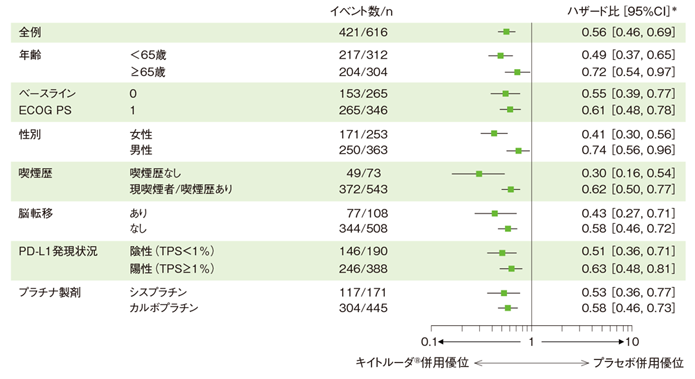
無増悪生存期間(PFS)のハザード比のフォレストプロット(ITT集団)
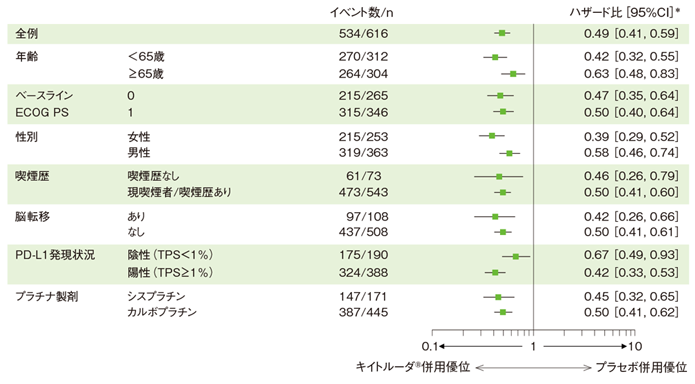
*投与群を共変量とし、PD-L1発現(≥1%、<1%)、プラチナ製剤(シスプラチン、カルボプラチン)、喫煙歴(喫煙歴なし、現喫煙者/喫煙歴あり)を層別因子とした層別Cox比例ハザードモデルに基づく
(追跡期間中央値:31.0ヵ月)(データカットオフ日:2019年5月20日)
Rodríguez-Abreu D et al. Ann Oncol 2021; 32: 881-895
本試験はMSD社の資金提供により行われた。
探索的評価項目 最終解析でのランダム化割り付けから2次治療での病勢進行、又は死亡のいずれかが先に起こるまでの期間:PFS2
PFS2*1のKaplan-Meier曲線(ITT集団)
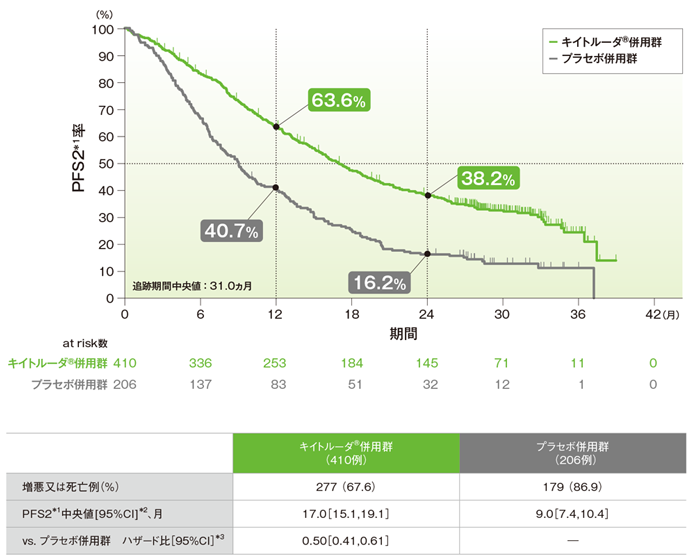
*1 ランダム化割り付けから2次治療での病勢進行、又は死亡のいずれかが先に起こるまでの期間
*2 打ち切りデータはproduct-limit(Kaplan-Meier)法に基づく
*3 投与群を共変量とし、PD-L1発現(≥1%、<1%)、プラチナ製剤(シスプラチン、カルボプラチン)、喫煙歴(喫煙歴なし、現喫煙者/喫煙歴あり)を層別因子とした層別Cox比例ハザードモデルに基づく
(追跡期間中央値:31.0ヵ月)(データカットオフ日:2019年5月20日)
Rodríguez-Abreu D et al. Ann Oncol 2021; 32: 881-895
本試験はMSD社の資金提供により行われた。
PFS2中央値は、キイトルーダ®併用群で17.0ヵ月(95%CI:15.1, 19.1)、プラセボ併用群で9.0ヵ月(95%CI:7.4, 10.4)でした。
副次評価項目 最終解析での奏効率:ORR
奏効率(ORR)の要約(ITT集団)
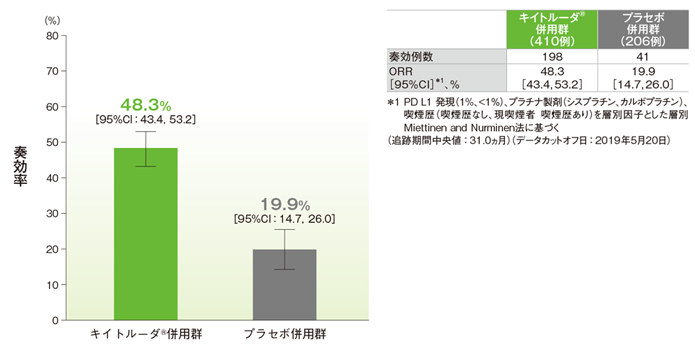
Rodríguez-Abreu D et al. Ann Oncol 2021; 32: 881-895
本試験はMSD社の資金提供により行われた。
ORRは、キイトルーダ®併用群で48.3%(95%CI:43.4, 53.2)、プラセボ併用群で19.9%(95%CI:14.7, 26.0)でした。
探索的評価項目(サブグループ解析) 最終解析でのPD-L1発現別の奏効率:ORR
PD-L1発現別の奏効率(ORR)の要約(ITT集団)
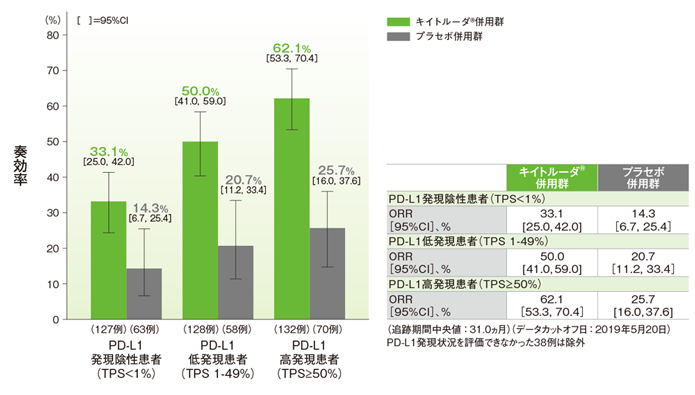
Rodríguez-Abreu D et al. Ann Oncol 2021; 32: 881-895
本試験はMSD社の資金提供により行われた。
副次評価項目 最終解析での奏効期間:DOR
奏効期間(DOR)の要約

*1 打ち切りデータはproduct-limit(Kaplan-Meier)法に基づく
*2 「+」は最後の疾患評価からPDがみられないことを示す
(追跡期間中央値:31.0ヵ月)(データカットオフ日:2019年5月20日)
Rodríguez-Abreu D et al. Ann Oncol 2021; 32: 881-895
本試験はMSD社の資金提供により行われた。
DOR中央値は、キイトルーダ®併用群で12.5ヵ月(範囲:1.1+, 34.9+)、プラセボ併用群で7.1ヵ月(範囲:2.4, 27.8+)でした。
最終解析での安全性
【重篤な副作用】1)
キイトルーダ®併用群:121例(29.9%) 内訳(2例以上):発熱性好中球減少症23例(5.7%)、血小板減少症13例(3.2%)、下痢、肺臓炎各11例(2.7%)、貧血10例(2.5%)、急性腎障害、好中球減少症各8例(2.0%)、大腸炎、肺炎、発熱各5例(1.2%)、蜂巣炎、悪心、汎血球減少症、嘔吐各4例(1.0%)、無力症、疲労、白血球減少症、尿細管間質性腎炎各3例 (0.7%)、自己免疫性肝炎、脱水、脳炎、全身健康状態低下、低マグネシウム血症、免疫性肝炎、感染症、腎炎、好中球減少性敗血症、末梢性浮腫、胸水、敗血症各2例(0.5%)
プラセボ併用群:44例(21.8%) 内訳(2例以上):貧血11例(5.4%)、血小板減少症6例(3.0%)、下痢5例(2.5%)、発熱性好中球減少症、嘔吐各4例(2.0%)、肺臓炎、悪心各3例(1.5%)、肺炎、汎血球減少症、ALT(GPT)上昇各2例(1.0%)
【投与中止に至った副作用】1)
キイトルーダ®併用群
キイトルーダ®の投与中止に至った副作用:71 例(17.5%) 内訳(2例以上):肺臓炎10例(2.5%)、急性腎障害、大腸炎各4例(1.0%)、慢性腎臓病、肝炎、腎炎、尿細管間質性腎炎各3例(0.7%)、ALT(GPT)上昇、自己免疫性肝炎、脳炎、疲労、発熱性好中球減少症、免疫性肝炎各2例(0.5%)
化学療法の投与中止に至った副作用:97例(24.0%) 内訳(2例以上):急性腎障害、肺臓炎各8例(2.0%)、下痢、疲労各5例(1.2%)、クレアチニン腎クリアランス減少、無力症、発熱性好中球減少症、腎不全各4例(1.0%)、血中クレアチニン増加、肝炎、末梢性浮腫、汎血球減少症、皮疹各3例(0.7%)、貧血、慢性腎臓病、食欲減退、免疫性肝炎、悪心、腎炎、尿細管間質性腎炎各2例(0.5%)
プラセボ併用群
プラセボの投与中止に至った副作用:11例(5.4%) 内訳(2例以上):肺臓炎、疲労各3例(1.5%)
化学療法の投与中止に至った副作用:18例(8.9%) 内訳(2例以上):疲労5例(2.5%)、肺臓炎2例(1.0%)
【死亡に至った副作用】2)
キイトルーダ®併用群:8例(2.0%) 内訳:急性腎障害、肺臓炎各2例、死亡(原因不明)、脳症、好中球減少性敗血症、肺炎各1例
プラセボ併用群:2例(1.0%) 内訳:肺炎、敗血症性ショック各1例
注)プラセボ併用群からクロスオーバー後、最初の投与後に生じた有害事象は除外した
(追跡期間中央値:31.0ヵ月)(データカットオフ日:2019年5月20日)
1)社内資料 KEYNOTE-189試験:安全性
2)Rodríguez-Abreu D et al. Ann Oncol 2021;32:881-895
Supplementary Data(Appendix)
本試験はMSD社の資金提供により行われた。
有害事象及び免疫関連など特に注目すべき有害事象一覧
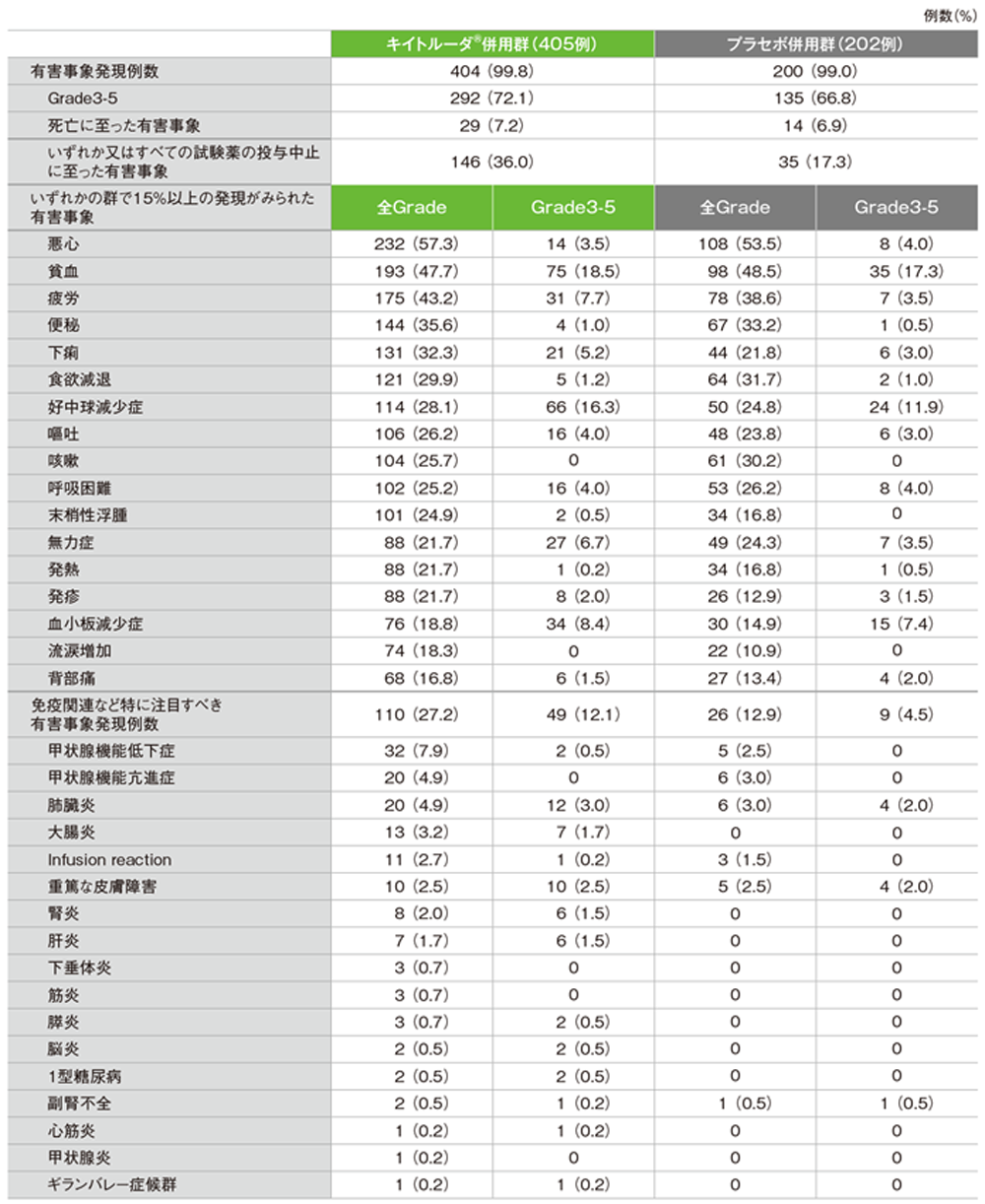
GradeはCTCAE version 4.0
(追跡期間中央値:31.0ヵ月)(データカットオフ日:2019年5月20日)
Rodríguez-Abreu D et al. Ann Oncol 2021;32:881-895
Supplementary Data(Appendix)
本試験はMSD社の資金提供により行われた。