KEYNOTE-010試験(5年間フォローアップ)
国際共同第Ⅱ/Ⅲ相試験:KEYNOTE-010試験(5年間フォローアップ)
探索的評価項目 5年間フォローアップでのPD-L1発現陽性患者(TPS≥1%)における全生存期間:OS
PD-L1発現陽性患者における全生存期間(OS)のKaplan-Meier曲線(ITT集団)
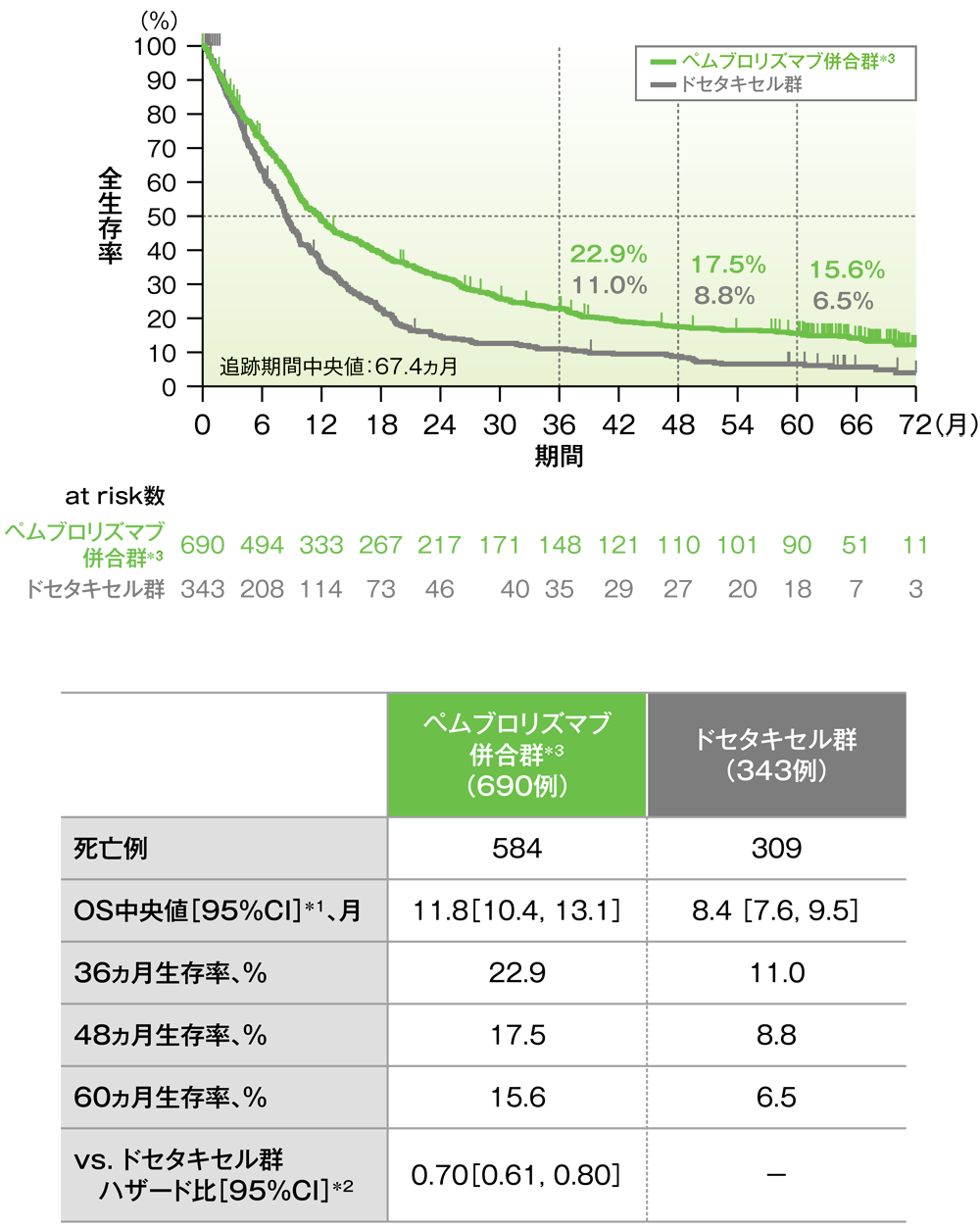
*1 打ち切りデータはproduct-limit(Kaplan-Meier)法に基づく
*2 投与群を共変量とし、ECOG PS(0、1)、治験実施医療機関の地域(東アジア、東アジア以外)、PD-L1発現(高発現、低発現、不明)を層別因子(無作為化に用いた層別因子)とした層別Cox比例ハザードモデルに基づく
*3 ペムブロリズマブ2mg/kg群とペムブロリズマブ10mg/kg群の併合群
(データカットオフ日:2020年4月8日)
Herbst RS et al. J Thorac Oncol 2021; 16: 1718-1732
本試験はMSD社の資金提供により行われた。
PD-L1発現陽性患者において、OS中央値は、キイトルーダ®併合群で11.8ヵ月(95%CI:10.4, 13.1)、ドセタキセル群で8.4ヵ月(95%CI:7.6, 9.5)でした。
探索的評価項目 5年間フォローアップでのPD-L1高発現患者(TPS≥50%)における全生存期間:OS
PD-L1高発現患者における全生存期間(OS)のKaplan-Meier曲線(ITT集団)
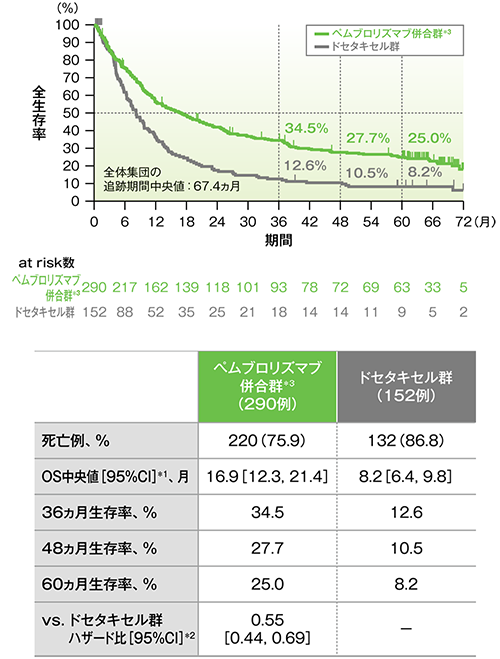
*1 打ち切りデータはproduct-limit(Kaplan-Meier)法に基づく
*2 投与群を共変量とし、ECOG PS(0、1)、治験実施医療機関の地域(東アジア、東アジア以外)、PD-L1発現(高発現、低発現、不明)を層別因子(無作為化に用いた層別因子)とした層別Cox比例ハザードモデルに基づく
*3 ペムブロリズマブ2mg/kg群とペムブロリズマブ10mg/kg群の併合群
(データカットオフ日:2020年4月8日)
Herbst RS et al. J Thorac Oncol 2021; 16: 1718-1732
本試験はMSD社の資金提供により行われた。
PD-L1高発現患者において、OS中央値は、キイトルーダ®併合群で16.9ヵ月(95%CI:12.3, 21.4)、ドセタキセル群で8.2ヵ月(95%CI:6.4, 9.8)でした。
サブグループ解析 5年間フォローアップでのPD-L1発現陽性患者(TPS≥1%)における部分集団因子別の全生存期間:OS
全生存期間(OS)のハザード比のフォレストプロット(キイトルーダ®併合群*1とドセタキセル群の比較、ITT集団)
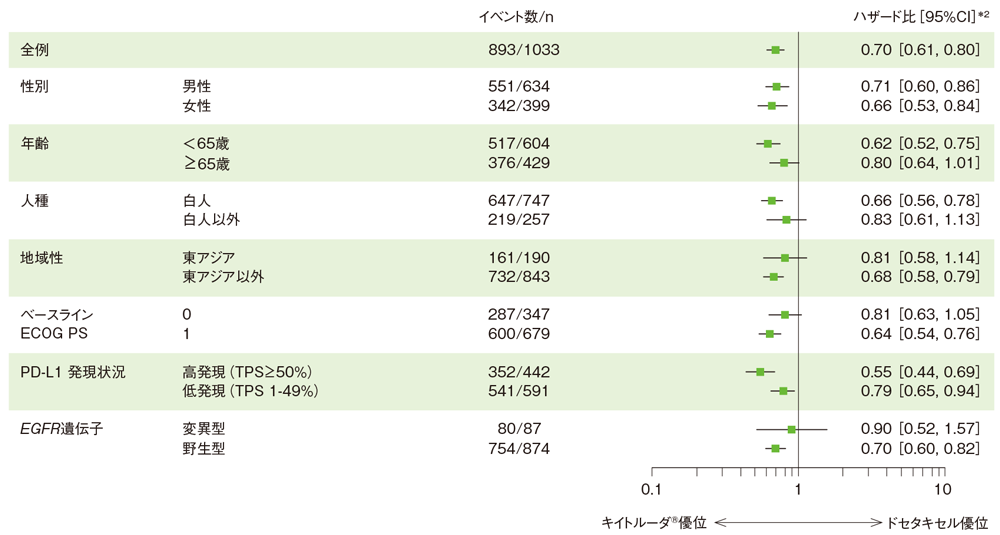
*1 キイトルーダ®2mg/kg群とキイトルーダ®10mg/kg群の併合群
*2 投与群を共変量とし、ECOG PS(0、1)、治験実施医療機関の地域(東アジア、東アジア以外)、PD-L1発現(高発現、低発現、不明)を層別因子とした層別Cox比例ハザードモデル
(追跡期間中央値:67.4ヵ月)
(データカットオフ日:2020年4月8日)
Herbst RS et al. J Thorac Oncol 2021; 16: 1718-1732
本試験はMSD社の資金提供により行われた。
探索的評価項目 5年間フォローアップでのPD-L1発現陽性患者(TPS≥1%)における無増悪生存期間:PFS
PD-L1発現陽性患者における無増悪生存期間(PFS)のKaplan-Meier曲線(ITT集団)
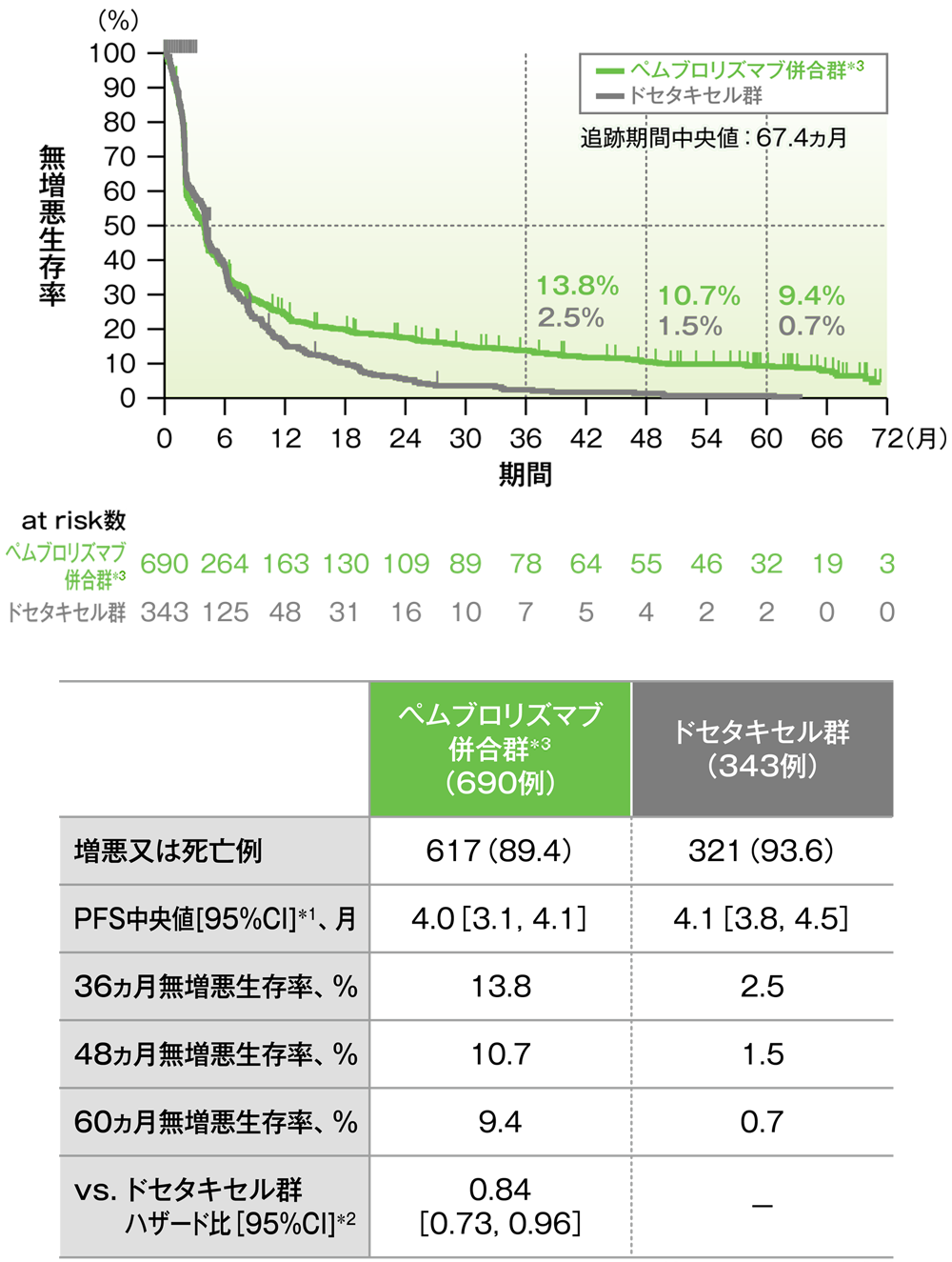
*1 打ち切りデータはproduct-limit(Kaplan-Meier)法に基づく
*2 投与群を共変量とし、ECOG PS(0、1)、治験実施医療機関の地域(東アジア、東アジア以外)、PD-L1発現(高発現、低発現、不明)を層別因子(無作為化に用いた層別因子)とした層別Cox比例ハザードモデルに基づく
*3 ペムブロリズマブ2mg/kg群とペムブロリズマブ10mg/kg群の併合群
(データカットオフ日:2020年4月8日)
Herbst RS et al. J Thorac Oncol 2021; 16: 1718-1732
本試験はMSD社の資金提供により行われた。
PD-L1発現陽性患者において、PFS中央値は、キイトルーダ®併合群で4.0ヵ月(95%CI:3.1, 4.1)、ドセタキセル群で4.1ヵ月(95%CI:3.8, 4.5)でした。
探索的評価項目 5年間フォローアップでのPD-L1高発現患者(TPS≥50%)における無増悪生存期間:PFS
PD-L1高発現患者における無増悪生存期間(PFS)のKaplan-Meier曲線(ITT集団)
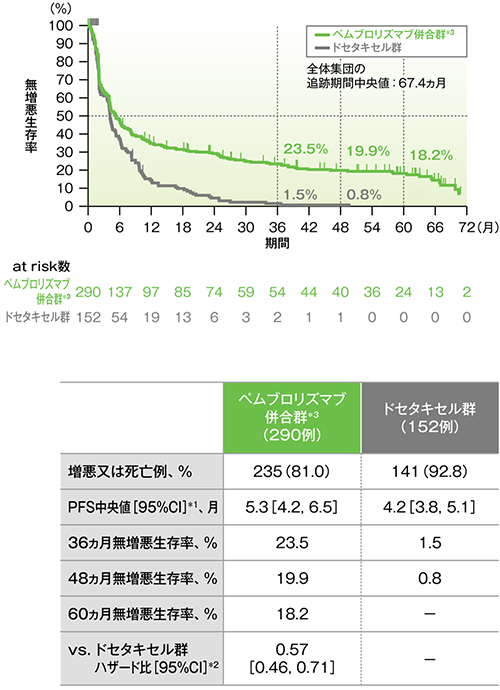
*1 打ち切りデータはproduct-limit(Kaplan-Meier)法に基づく
*2 投与群を共変量とし、ECOG PS(0、1)、治験実施医療機関の地域(東アジア、東アジア以外)、PD-L1発現(高発現、低発現、不明)を層別因子(無作為化に用いた層別因子)とした層別Cox比例ハザードモデルに基づく
*3 ペムブロリズマブ2mg/kg群とペムブロリズマブ10mg/kg群の併合群
(データカットオフ日:2020年4月8日)
Herbst RS et al. J Thorac Oncol 2021; 16: 1718-1732
本試験はMSD社の資金提供により行われた。
5年間フォローアップでの35サイクルの治療完遂例について
患者背景
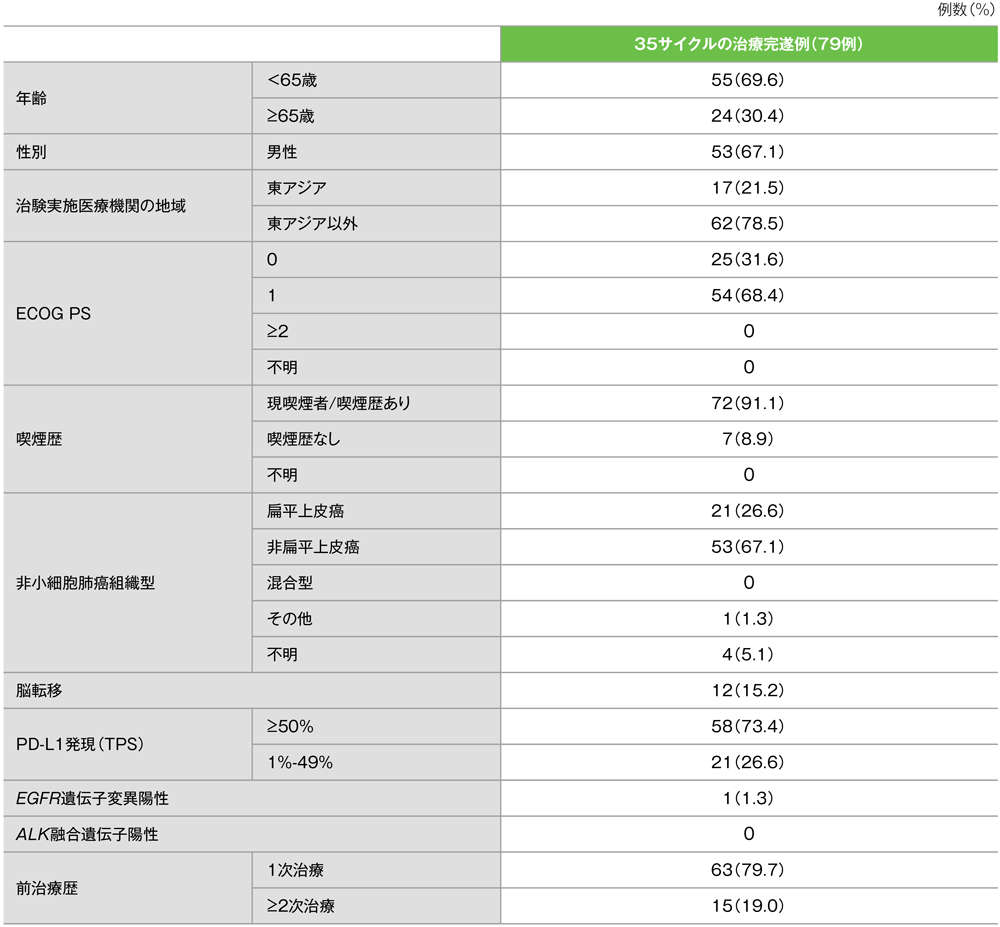
Herbst RS et al. J Thorac Oncol 2021; 16: 1718-1732
本試験はMSD社の資金提供により行われた。
5年間フォローアップでの35サイクルの治療完遂例における奏効率(ORR)

(追跡期間中央値:67.4ヵ月)(データカットオフ日:2020年4月8日)
Herbst RS et al. J Thorac Oncol 2021; 16: 1718-1732
本試験はMSD社の資金提供により行われた。
5年間フォローアップでのキイトルーダ®による投与第2期実施例について
患者背景
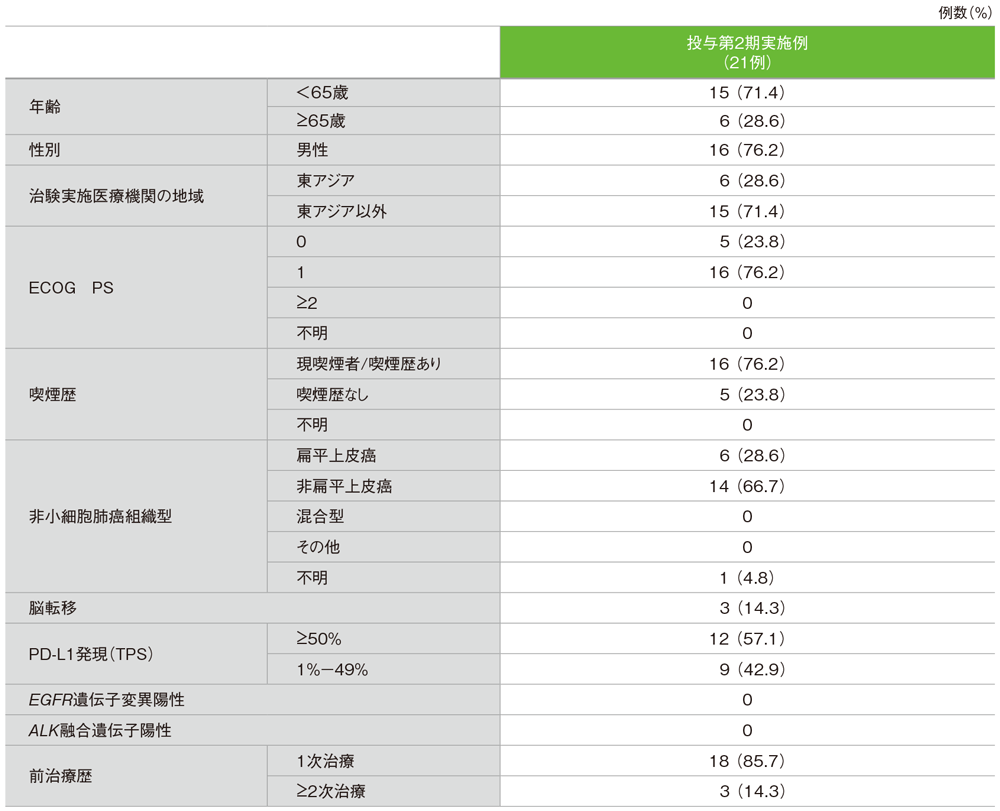
Herbst RS et al. J Thorac Oncol 2021; 16: 1718-1732
本試験はMSD社の資金提供により行われた。
5年間フォローアップでのキイトルーダ®による投与第2期実施例における奏効率(ORR)

(追跡期間中央値:67.4ヵ月)(データカットオフ日:2020年4月8日)
Herbst RS et al. J Thorac Oncol 2021; 16: 1718-1732
本試験はMSD社の資金提供により行われた。
主要評価項目 5年間フォローアップでの主な副作用*1(APaT集団)
【副作用】
キイトルーダ®併合群*2 :462/682例(67.7%)
ドセタキセル群:255/309例(82.5%)
【Grade 3-5の副作用】
キイトルーダ®併合群*2 :110例(16.1%)
ドセタキセル群:113例(36.6%)
【投与中止に至った副作用】
キイトルーダ®併合群*2 :40例(5.9%)
ドセタキセル群:37例(12.0%)
【死亡に至った副作用】*3
キイトルーダ®併合群*2 :5例(0.7%) 内訳:肺臓炎3例、心筋梗塞、肺炎各1例
ドセタキセル群:5例(1.6%) 内訳:発熱性好中球減少症、急性心不全、気道感染、脱水、間質性肺疾患各1例
*1 論文中に、重篤な副作用、投与中止に至った副作用の具体的な事象名の記載なし
*2 キイトルーダ®2mg/kg群とキイトルーダ®10mg/kg群の併合群
*3 3年間フォローアップと同様
(データカットオフ日:2020年4月8日)
Herbst RS et al. J Thorac Oncol 2021; 16: 1718-1732
本試験はMSD社の資金提供により行われた。
副作用及び免疫関連など特に注目すべき有害事象一覧
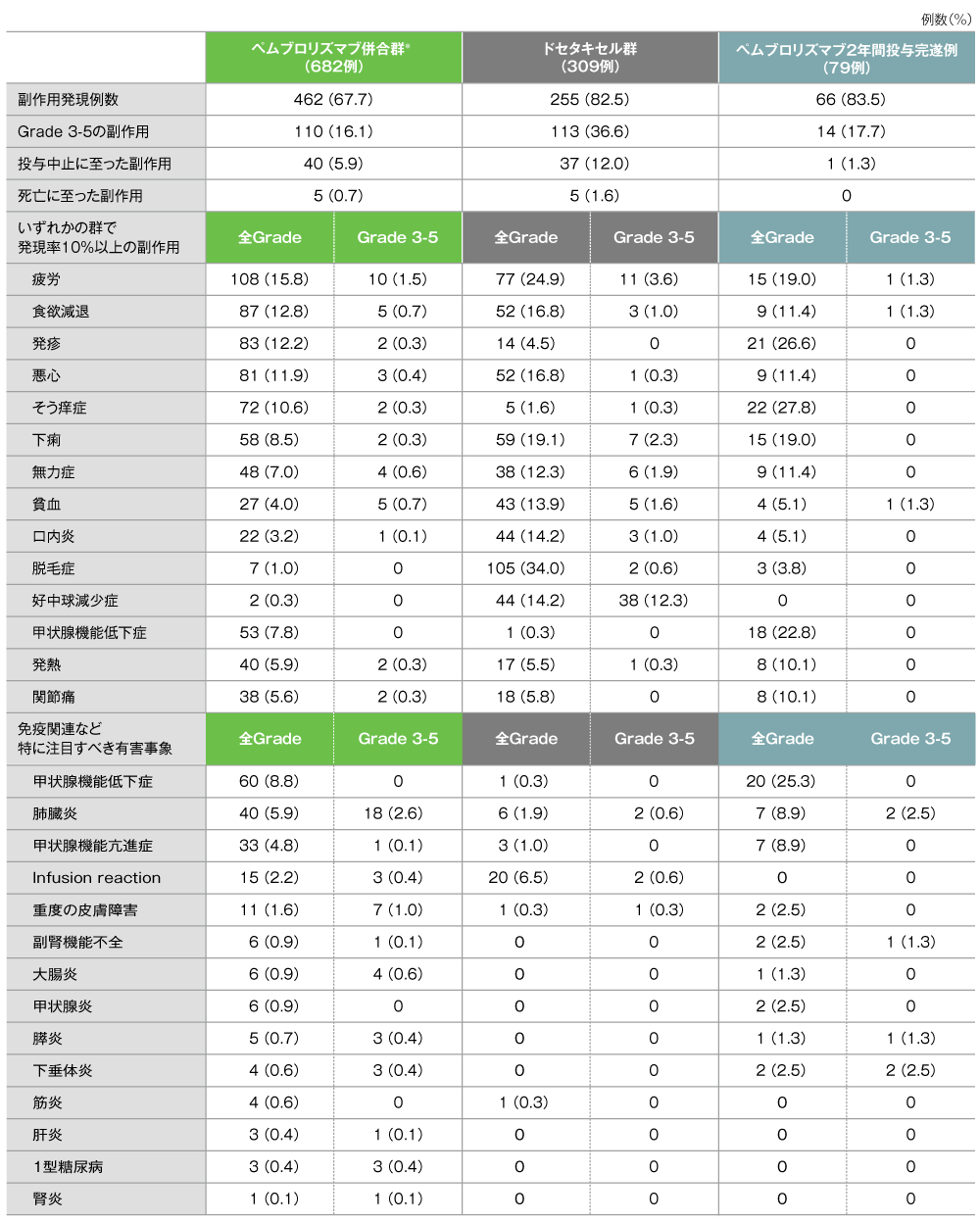
GradeはCTCAE version 4.0
*キイトルーダ®2mg/kg群とキイトルーダ®10mg/kg群の併合群
(追跡期間中央値:67.4ヵ月)(データカットオフ日:2020年4月8日)
Herbst RS et al. J Thorac Oncol 2021; 16: 1718-1732
本試験はMSD社の資金提供により行われた。


