薬効薬理:非臨床試験
薬効薬理:非臨床試験
1. 抗ウイルス作用1)
(1)AD169感染NHDF細胞における抗ヒトCMV作用(in vitro)
レテルモビルはヒトCMV DNAの複製に影響を及ぼしませんでしたが、ヒトCMVの感染性粒子の産生を抑制しました。
■ヒトCMV DNAの複製(A)及び感染性粒子の産生(B)に対する作用
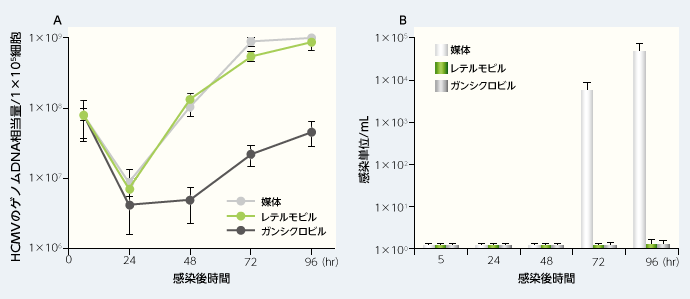
方法:正常ヒト皮膚線維芽(NHDF)細胞にAD169株を感染多重度(MOI)=0.1で感染させ、それぞれ50%作用濃度(EC50値)の約10倍濃度のレテルモビル(50nM)、ガンシクロビル(20μM)又は媒体(ジメチルスルホキシド、DMSO)の存在下で96時間培養し、感染ウイルス量を定量した。
(2)各種ヒトCMV株感染における抗ヒトCMV作用(in vitro)
ヒトCMVの各種臨床分離株及び実験室株に対するレテルモビルの抗ウイルス作用を、感染細胞培養系にて検討した結果、ガンシクロビルに耐性の実験室株を含むすべてのヒトCMV株はレテルモビルに対して感受性を示し、そのEC50値は0.0018~0.0061μMでした。
■各種HCMV株に対する抗ウイルス作用
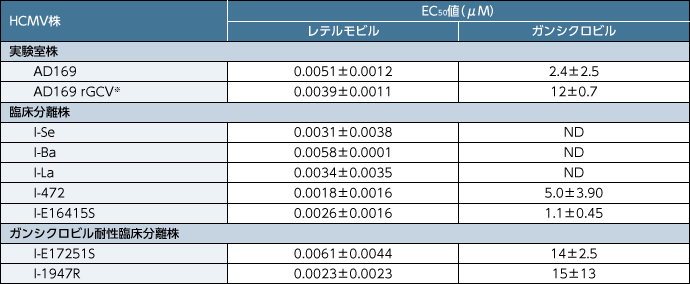
平均値±SD(n≥2)
※:ガンシクロビル(GCV)の耐性株
ND:試験をせず
方法:正常ヒト皮膚線維芽(NHDF)細胞に各種ヒトCMV株を感染させ、種々の濃度の被験薬物又は媒体(DMSO)の存在下で6~7日間培養した。ギムザ染色を行い、被験薬物を含まないウイルスのみの対照ウェルと比較して50%の細胞変性効果を示す被験薬物濃度(EC50値)を算出した。
(3)ウイルスに対する選択性(in vitro)
ヒトCMV以外の各種ヒト病原性ウイルスに対するレテルモビルの抗ウイルス作用を感染細胞培養系にて検討しました。
①ヘルペスウイルスに対する抗ウイルス作用
ヘルペスウイルスであるアルファヘルペスウイルス(水痘・帯状疱疹ウイルス、単純ヘルペスウイルス1型及び2型)、ベータヘルペスウイルス(マウスCMV、ラットCMV及びヒトヘルペスウイルス6)、並びにガンマヘルペスウイルス(Epstein-Barrウイルス)に対するレテルモビルの抗ウイルス作用を検討した結果、レテルモビルの抗ウイルス作用はヒトCMVに選択的でした。レテルモビルのマウスCMVに対するEC50値は高値であり、それら以外の試験をしたいずれのウイルスに対してもレテルモビルは抗ウイルス作用を示しませんでした。
②ヘルペスウイルス以外の主要なウイルスに対する抗ウイルス作用
ヒトアデノウイルス2、B型肝炎ウイルス、ヒト免疫不全ウイルス1、A型インフルエンザウイルス及びC型肝炎ウイルスのレテルモビルに対する感受性について検討した結果、レテルモビルは、検討したいずれのウイルスに対しても抗ウイルス作用を示さず、ヒトCMVに選択的でした。
2. 耐性ウイルス
(1)細胞培養系(in vitro)1)
CMVのDNAターミナーゼのサブユニットはCMV遺伝子のUL51、UL56及びUL89領域にコードされます。細胞培養系にてレテルモビルに低感受性のCMV変異株を分離しました。その結果、pUL51(P91S、A95V)、pUL56(C25F、S229F、V231A/L、N232Y、V236A/L/M、E237D、L241P、T244K/R、L254F、L257F/I、K258E、F261C/L/S、Y321C、C325F/R/W/Y、L328V、M329T、A365S、N368D、R369G/M/S)及びpUL89(N320H、D344E)にアミノ酸置換が認められました。これらの置換を有する遺伝子組換えCMV 変異株のEC50値は野生株と比較して1.6~9,300倍高値を示しました。
(2)成人同種造血幹細胞移植患者を対象とした臨床試験2、3、4)
外国人を対象とした第Ⅱ相試験(020試験)では、131例の成人同種造血幹細胞移植患者に60、120又は240mgのレテルモビル又はプラセボを1日1回84日間投与し、レテルモビル群のうち予防不成功*となり検体が得られた12例を対象に、UL56遺伝子の231~369位のアミノ酸配列を中心にDNAシークエンス解析を実施しました。60mg投与群1例でレテルモビルに低感受性を示す置換(V236M)が検出されました。
成人同種造血幹細胞移植患者を対象とした第Ⅲ相国際共同試験(001試験)では、レテルモビル群のうち予防不成功となり検体が得られた50例を対象に、UL56及びUL89遺伝子のすべてのコード領域のDNAシークエンス解析を実施しました。3例でレテルモビルに低感受性を示す4種類の置換がpUL56に検出されました。1例でC325W及びR369Tが、他の2例で各々V236M及びE237Gの置換が検出されました。
成人同種造血幹細胞移植患者を対象とした第Ⅲ相国際共同試験(040試験)では、全投与群のうち予防不成功又は早期中止しCMV血症が認められた32例を対象に、UL51、UL56及びUL89遺伝子のすべてのコード領域のDNAシークエンス解析を実施しました。レテルモビルに低感受性を示す置換は検出されませんでした。
*:プレバイミス®の効能又は効果は、「下記におけるサイトメガロウイルス感染症の発症抑制 〇同種造血幹細胞移植 〇臓器移植」である。
(3)成人腎移植患者を対象とした臨床試験5、6)
外国人成人腎移植患者を対象とした第Ⅲ相海外試験(002試験)では、レテルモビル群のうちCMV感染症を発症又は早期中止しCMV血症が認められ検体が得られた52例を対象に、UL51、UL56及びUL89遺伝子のすべてのコード領域のDNAシークエンス解析を実施しました。レテルモビルに低感受性を示す置換は検出されませんでした。
日本人成人腎移植患者を対象とした第Ⅲ相国内試験(042試験)では、レテルモビルの投与を受けた患者のうちCMV感染症を発症又はCMV血症が認められ検体が得られた4例を対象に、UL51、UL56及びUL89遺伝子のすべてのコード領域のDNAシークエンス解析を実施しました。レテルモビルに低感受性を示す置換は検出されませんでした。
(4)小児同種造血幹細胞移植患者を対象とした臨床試験7)
小児同種造血幹細胞移植患者を対象とした後期第Ⅱ相国際共同試験(030試験)では、CMV血症が認められ検体が得られた10例を対象に、UL51、UL56及びUL89遺伝子のすべてのコード領域のDNAシークエンス解析を実施しました。2例でレテルモビルに低感受性を示す置換がpUL56に検出されました。1例でR369Sが、他の1例でC325Wの置換が検出されました。
3. 交差耐性(in vitro)1)
ガンシクロビルに耐性を示すpUL97またはpUL54領域に置換を有するCMV は、レテルモビルに感受性を示しました。野生型と比較してガンシクロビルに対する感受性を2.1倍低下させるpUL56 E237G置換を有する遺伝子組換えCMV株を除き、レテルモビルに対し耐性を示す置換を有する各種遺伝子組換え株は、ホスカルネット及びガンシクロビルに対して感受性を示しました。
1)社内資料(in vitro薬効薬理試験)
2)承認時評価資料(第Ⅲ相国際共同試験:001試験)
3)承認時評価資料(後期第Ⅱ相用量反応試験:020試験)
4)電子添文改訂時評価資料(第Ⅲ相国際共同試験:040試験)
5) 適応追加(臓器移植)承認時評価資料(第Ⅲ相海外共同試験:002試験)
6) 適応追加(臓器移植)承認時評価資料(第Ⅲ相国内試験:042試験)
7)用法及び用量追加(小児)承認時評価資料(後期第Ⅱ相国際共同試験:030試験)