シベクトロ®に関する過去のお知らせ一覧
過去のお知らせ一覧

本試験の対象には一部国内承認外の適応菌種が含まれるデータで評価され承認されたため、国内で承認されている効能又は効果と異なるデータも紹介しています。
承認時評価資料:急性細菌性皮膚・皮膚組織感染症患者を対象とした第Ⅲ相試験(ESTABLISH-2;TR701-113試験)
Moran GJ, et al.:Lancet Infection Dis. 2014;14(8):696-705.
[利益相反:本試験は、キュビスト社(現MSD)が実施した。F.E.、A.C.D.、P.P.はキュビスト社(現MSD)の社員。]
投与開始後48~72時間の早期臨床効果(有効率)は、シベクトロ®群(6日間投与)85.2%、リネゾリド群(10日間投与)82.6%であり、シベクトロⓇ群はリネゾリド群に対して非劣性であることが検証されました。
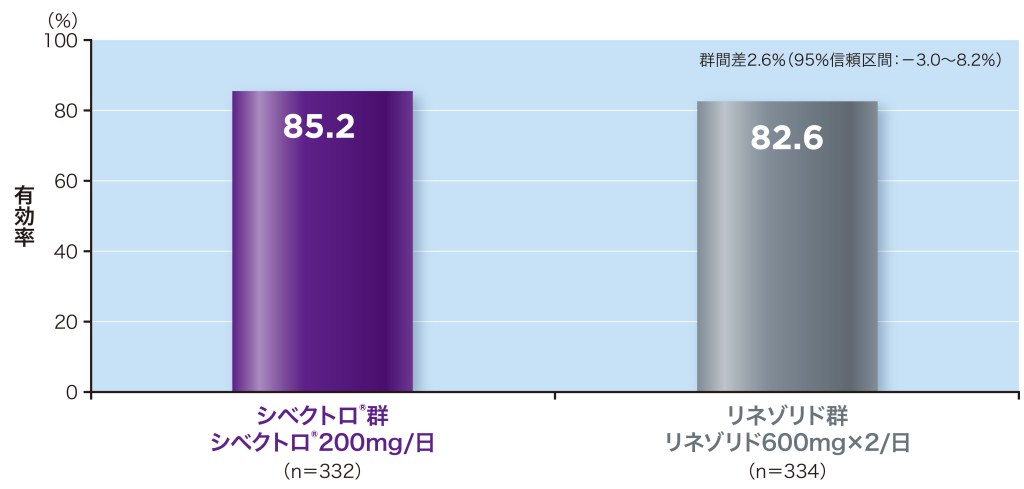
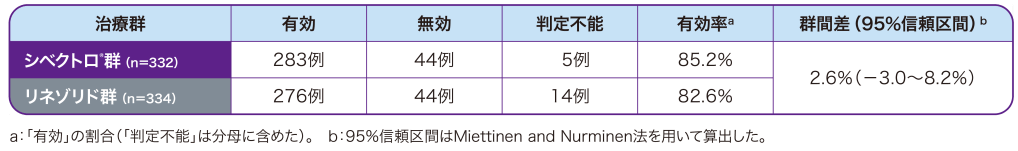
以下の基準に基づき、臨床効果をプログラム判定した。
| 判定 | 判定基準 |
| 有効 | 治験薬投与開始後48~72時間に急性細菌性皮膚・皮膚組織感染症の主病変(紅斑、浮腫又は硬結)の面積(長さ×幅) がベースラインから20%以上縮小 |
| 無効 | 以下のいずれかに該当する場合 ● 治験薬投与開始後48~72時間の急性細菌性皮膚・皮膚組織感染症の主病変面積のベースラインからの縮小が20%未満 ● 治験薬投与開始後72時間までに、ベースライン時の原因菌に有効とされる全身性抗菌薬(創感染患者でのアズトレオナム又はメトロニダゾールによる補助投与を除く)を併用 ● 治験薬投与開始後72時間までの死亡(原因は問わない) |
副作用は、シベクトロ®群331例中68例(20.5%)、リネゾリド群327例中81例(24.8%)に認められました。
主な副作用(発現率2%以上)は、シベクトロ®群で悪心(21例、6.3%)、嘔吐(9例、2.7%)、下痢、疲労、頭痛(いずれも7例、2.1%)、リネゾリド群で悪心(27例、8.3%)、下痢(15例、4.6%)、嘔吐(14例、4.3%)、頭痛(10例、3.1%)でした。
重篤な副作用は、リネゾリド群でアナフィラキシー反応(1例、0.3%)が認められ、シベクトロ®群では認められませんでした。
シベクトロ®群の1例が心筋梗塞により第15日に死亡し、リネゾリド群の1例が結核性髄膜炎により第20日に死亡しました(いずれも治験薬との因果関係なし)。
投与中止に至った有害事象は、シベクトロ®群で1例[腹部不快感1例](0.3%)、リネゾリド群で4例[頭痛2例、視力低下、悪心、嘔吐、疼痛、発熱、アナフィラキシー反応、落ち着きのなさ各1例](1.2%)に認められました。
試験:国際共同、リネゾリド対照、無作為化、二重盲検、ダブルダミー比較試験(非劣性試験、検証試験)
目的:急性細菌性皮膚・皮膚組織感染症患者を対象として、シベクトロⓇ6日間投与のリネゾリド10日間投与(いずれも点滴静注から経口投与への切り替え可)に対する非劣性を、投与開始後48~72時間のプログラム判定による早期臨床効果(有効率、ITT※1にて評価)について検証する。
対象:12歳以上の急性細菌性皮膚・皮膚組織感染症患者[ITT解析対象例数:666例(シベクトロ®群332例、リネゾリド群334例)]
方法:対象患者を、シベクトロ®群又はリネゾリド群に1:1の比で無作為割り付けし、シベクトロ®群にはシベクトロ®200mgを1日1回6日間、リネゾリド群にはリネゾリド600mgを1日2回10日間、ダブルダミー法にて点滴静注により投与を開始した。投与に際しては、少なくとも最初の2回(プラセボを含む)は点滴静注とし、その後事前に規定した基準を満たした場合は経口投与へ切り替えができることとした(全て点滴静注にすることも可能)。
| 評価項目: | 〈主要評価項目〉投与開始後48~72時間のプログラム判定による早期臨床効果(有効率、ITTにて評価)[検証的解析項目] 〈副次評価項目〉投与終了(EOT)時(第11日)のプログラム判定による臨床効果(治癒率)、投与終了後評価(PTE)時(EOT後7~14日)の治験責任(分担)医師評価による臨床効果(治癒率)、投与開始後48~72時間及び第7日の治験責任(分担)医師評価による臨床効果、各評価時点の疼痛スコアのベースラインからの変化 〈安全性の評価項目〉有害事象、臨床検査(血液学的検査及び血液生化学検査)、バイタルサイン(血圧、心拍数、呼吸数及び体温)、ECG、理学的検査(脳神経系を含む基本的な神経学的検査)、視力検査 |
| 解析計画: | 有効性の主要評価項目及び副次評価項目における臨床効果では、有効率(「有効」の割合)について、群間差(シベクトロ®群-リネゾリド群)の両側95%信頼区間を算出した。また、第1種の過誤の確率を制御するため、Westfall and Krishenの逐次的検定手順を使用し、主要評価項目についてシベクトロ®群の非劣性が検証された場合、副次評価項目について事前に規定した順序で非劣性の検定を行うこととした。群間差(シベクトロ®群-リネゾリド群)の両側95%信頼区間の下限値が-10%より大きかった場合、リネゾリドに対するシベクトロ®の非劣性が成り立つとした。また、MRSA患者の部分集団解析は事前に計画されていなかったが、PTE時の治験責任(分担)医師による臨床効果の検討を行い、評価資料として評価された。安全性の解析は、安全性解析対象集団(SAF※2)を対象とした。 |
※1 ITT:割り付けられた全ての患者
※2 SAF:ITTのうち、割り付け後に治験薬を少なくとも1回以上投与された患者
シベクトロ®の4.効能又は効果
< 適応菌種>テジゾリドに感性のメチシリン耐性黄色ブドウ球菌(MRSA)
<適応症>深在性皮膚感染症、慢性膿皮症、外傷・熱傷及び手術創等の二次感染、びらん・潰瘍の二次感染
シベクトロ®の6.用法及び用量
(シベクトロ®錠200mg)通常、成人にはテジゾリドリン酸エステルとして200mgを1日1回経口投与する。
(シベクトロ®点滴静注用200mg) 通常、成人にはテジゾリドリン酸エステルとして200mgを1日1回、1時間かけて点滴静注する。
シベクトロ®の9. 特定の背景を有する患者に関する注意(抜粋)
9.7 小児等
小児等を対象とした臨床試験は実施していない。
リネゾリドの4.効能又は効果(詳細は製品電子添文をご参照ください。)
<適応菌種>本剤に感性のメチシリン耐性黄色ブドウ球菌(MRSA)
<適応症>敗血症、深在性皮膚感染症、慢性膿皮症、外傷・熱傷及び手術創等の二次感染、肺炎
<適応菌種>本剤に感性のバンコマイシン耐性エンテロコッカス・フェシウム
<適応症>各種感染症
WEB講演会にアクセスし「このページは閲覧を制限しています」と表示された方は こちら>>
このサイトでは、医療用医薬品を適正にご使用いただくため、医師、歯科医師及び薬剤師などの医療関係者の方を対象に、主としてMSD株式会社の医療用医薬品に関する情報を提供しています。
下記の「はい」をクリックした場合、「MSD Connect ご利用規約」及び「ウェブサイトのご利用条件」を理解したうえで、内容に同意したものとみなします。
2024年11月にご利用規約を改訂致しました。上記リンクよりご確認ください。
あなたは医療関係者ですか?