薬物動態 血漿中濃度(生物学的同等性試験)
薬物動態 血漿中濃度(生物学的同等性試験)
投与0時間から48時間後までの血漿中薬物濃度−時間曲線下面積(AUC0-48hr)および最高血漿中薬物濃度(Cmax)の幾何平均比(配合剤/単剤併用)[90%信頼区間]は、シタグリプチンでそれぞれ0.99[0.98, 1.00]および0.97[0.93,1.02]、イプラグリフロジンでそれぞれ0.99[0.97, 1.01]および1.02[0.94, 1.10]でした。
シタグリプチンおよびイプラグリフロジンのAUC0-48hrおよびCmaxの幾何平均比の90%信頼区間は、いずれも生物学的同等性の評価基準である[0.80, 1.25]の範囲に含まれていたことから、スージャヌ®配合錠は、シタグリプチン50mgおよびイプラグリフロジン50mg併用と生物学的に同等であると判定されました。
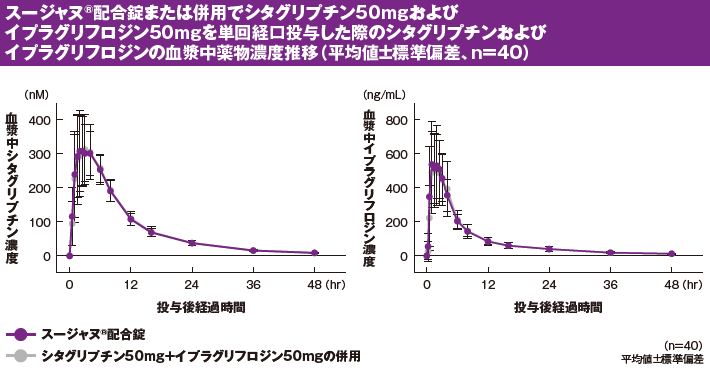
国内第Ⅰ相臨床試験P855(承認申請時評価資料)
健康成人におけるスージャヌ®配合錠または
シタグリプチン50mg・イプラグリフロジン50mg併用投与後の
シタグリプチン薬物動態パラメータ
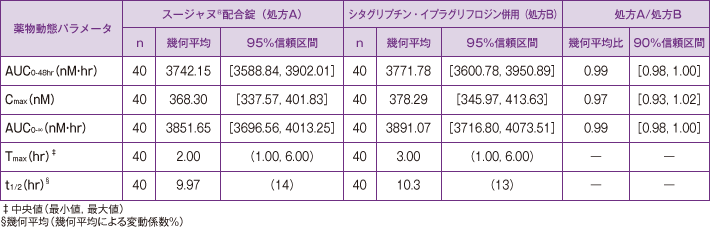
健康成人におけるスージャヌ®配合錠または
シタグリプチン50mg・イプラグリフロジン50mg併用投与後の
イプラグリフロジン薬物動態パラメータ
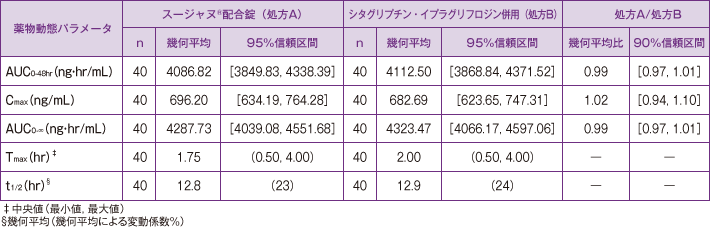
試験概要
対 象
健康成人男性40例
方 法
対象を無作為に2群(各群20例)に割り付け、クロスオーバー法により、各投与期にスージャヌ®配合錠、またはシタグリプチン50mgおよびイプラグリフロジン50mg各単剤を併用で空腹時に単回経口投与した。
「禁忌」等その他項目はこちらをご参照ください。