臨床成績
臨床成績
日本人を含む国際共同第Ⅲ相試験(019試験:PNEU-AGE)
本剤の承認されている効能又は効果は、「高齢者又は肺炎球菌による疾患に罹患するリスクが高いと考えられる者における肺炎球菌(血清型1、3、4、5、6A、6B、7F、9V、14、18C、19A、19F、22F、23F及び33F)による感染症の予防」である。
本試験では、一部承認外の接種者が含まれるが、承認時評価資料として評価されたため掲載する。
承認時評価資料:国際共同第Ⅲ相試験(019試験)
Platt HL, et al. Vaccine. 2022;40:162-172.
Kishino H, et al. Jpn J Infect Dis. 2022;75(6):575-582.
【利益相反】本研究はMSD社からの資金提供により実施され、著者には同社の社員が含まれている。
試験デザイン
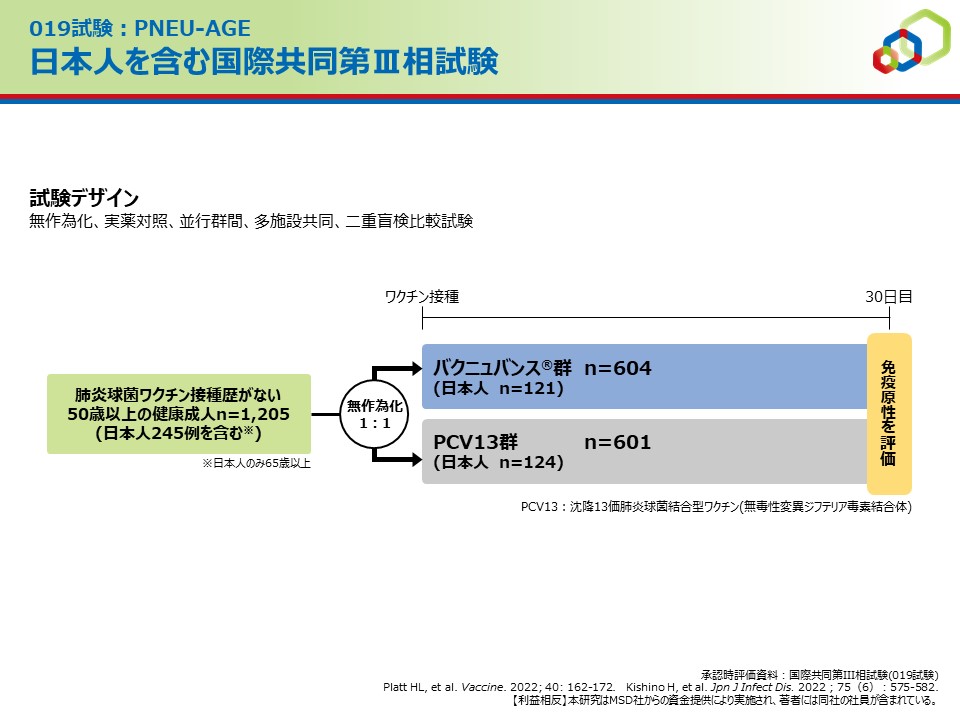
試験概要

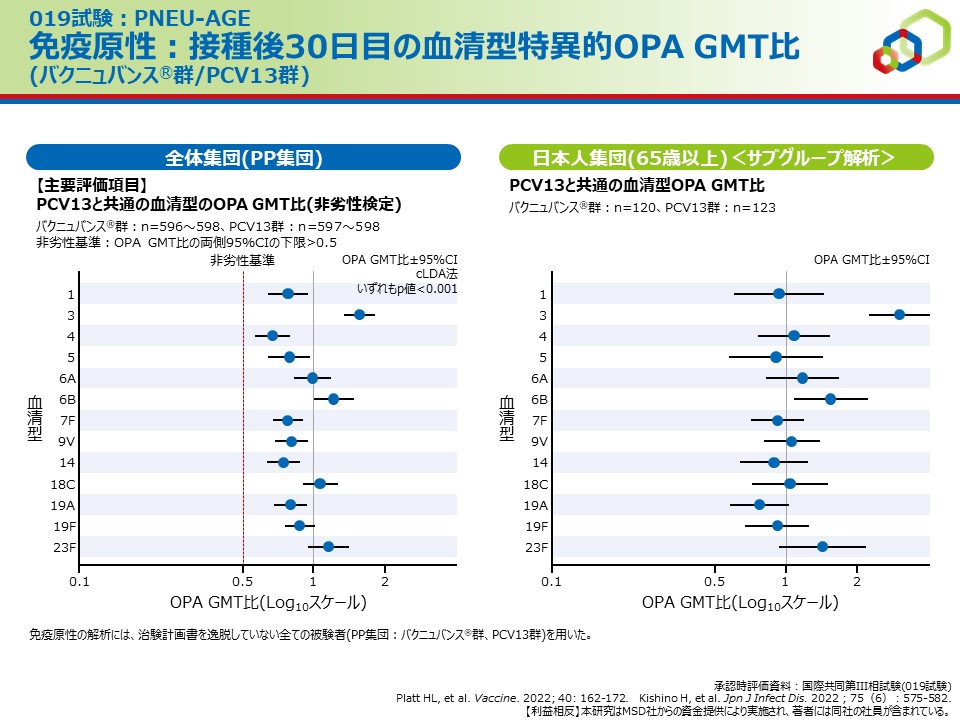
免疫原性: PCV13と共通の血清型のOPA GMT比
【主要評価項目】
50歳以上の肺炎球菌ワクチン接種歴がない成人を対象とした試験で、全体集団(PP集団)においてバクニュバンス®群はオプソニン活性(OPA)の幾何平均力価(GMT)においてPCV13と共通の血清型でPCV13群に対する非劣性及びバクニュバンス®固有の2血清型でPCV13群に対する優越性が検証されました。
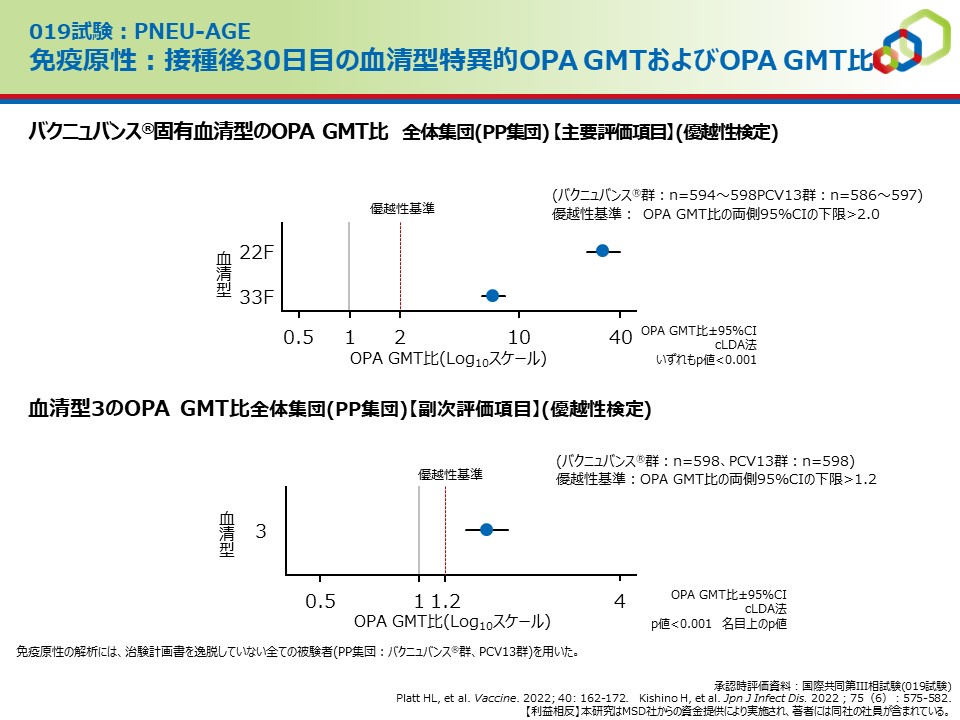
免疫原性:接種後30日目の血清型特異的OPA GMTおよびOPA GMT比
バクニュバンス®固有血清型のOPA GMT比 全体集団(PP集団) 【主要評価項目】(優越性検定)
バクニュバンス®群の血清型特異的オプソニン活性(OPA)の幾何平均抗体価(GMT)は、
バクニュバンス®固有の2血清型(22Fおよび33F)ではPCV13群に対する優越性が検証された。
血清型3のOPA GMT比全体集団(PP集団)【副次評価項目】(優越性検定)
血清型3においてPCV13群に対する優越性が示された。
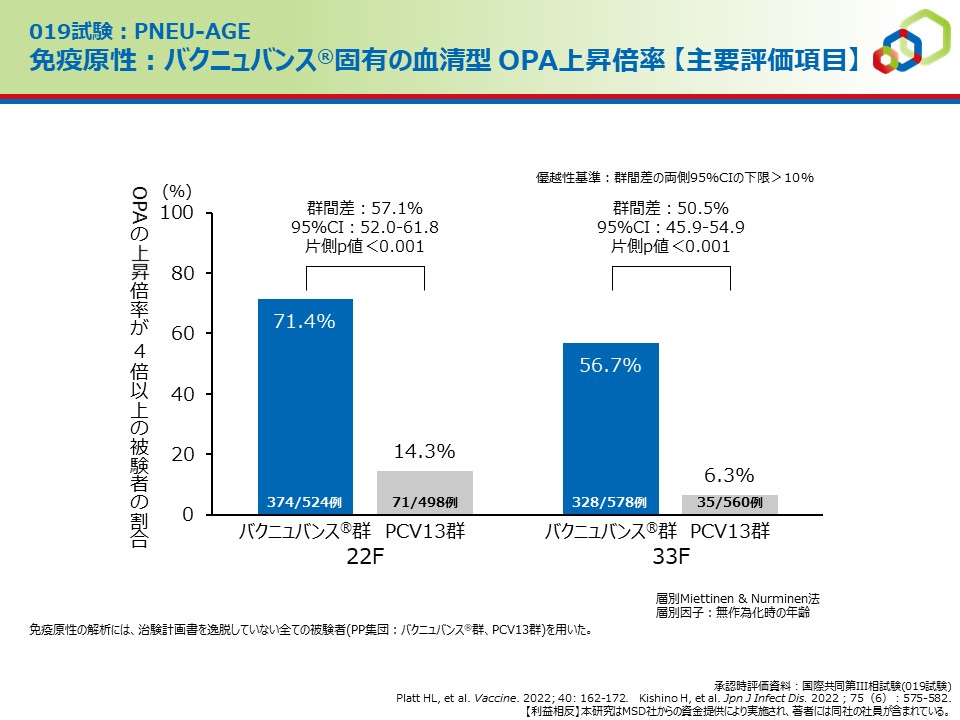
免疫原性:バクニュバンス®固有の血清型 OPA上昇倍率
【主要評価項目】
50歳以上の肺炎球菌ワクチン接種歴がない成人を対象とした試験で、バクニュバンス®固有の2血清型における血清型特異的オプソニン活性(OPA)応答の上昇倍率が4倍以上であった被験者割合の群間差は、血清型22Fでは57.1%、血清型33Fでは50.5%であり、バクニュバンス®固有の2血清型においてPCV13群に対するバクニュバンス®群の優越性が検証されました。
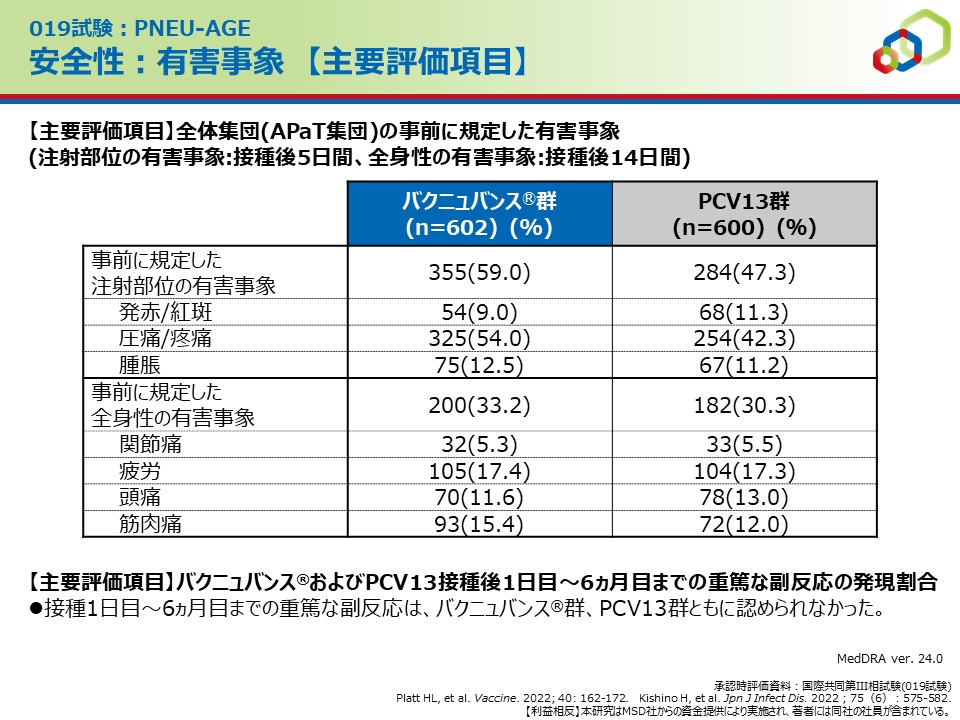
安全性
019試験の安全性の結果は下記の通りです。